Константа - образование - комплекс
Cтраница 1
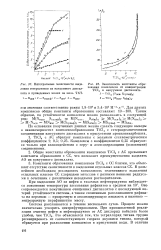 |
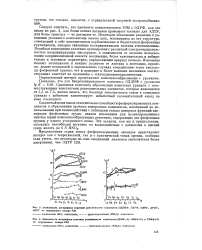
Интегральные зависимости выде - [ IMAGE ] Зависимость константы обра. [1] |
Константы образования комплексов Т1С14 с СС близки, это объясняет отсутствие селективности в выделении отдельных классов СС. В дальнейшем необходимо исследовать возможность селективного выделения отдельных классов СС хлоридами металлов с разными ионными радиусами в сочетании с различными неводными растворителями. [2]
Константа образования комплекса металл - индикатор ( / Смш) в рабочем интервале рН должна быть большой ( 104) для того, чтобы индикатор соответствовал своему назначению и для получения наименьшей ошибки титрования. [3]
Константы образования комплексов с 13 и другими реагентами в большинстве случаев определяются основностью лигандов и стери-ческими факторами. [4]
Константы образования комплексов убывают в ряду лигандов SH OHNH2, что указывает на предпочтительную связь Mo ( V) с серусодержащими лигандами. [5]
Константы образования комплексов ( см. разд. [6]
Константы образования комплексов молибдена с ЭДТА состава 1: 1 [108, 111, 112] близки по величине к константам комплексов с метилиминодиуксусной кислотой [112, 113], что подтверждает правильность предложенной структуры. [7]
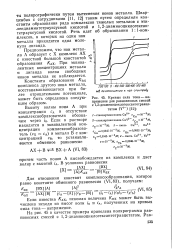 |
Кривые сила тока - напряжение для равновесных смесей с 1 2-диаминоциклогексантетрааце-татом ( Y4 -. [8] |
Константа образования Къх комплекса другого иона металла, восстанавливающегося при более отрицательном потенциале, может быть определена следующим образом. [9]
Некоторые константы образования комплексов плутония ( IV) приведены в табл. 7.2. Среди многих не перечисленных комплексов, образуемых ионом Ри4, имеется ряд фосфатных комплексов и два очень устойчивых и сильно окрашенных двухатомных пероксидных комплекса. Достойны внимания большое сродство иона Ри к очень маленькому фторид-иону и заметная степень комплексообразования его с хлоридом и нитратом. При высоких концентрациях НМОз или НС1 плутоний ( IV) образует анионные комплексы, хорошо сорбирующиеся сильноосновкыми анионитами. Эти комплексы образуются при концентрации НС. [10]
Логарифмы констант образования комплекса, отнесенные к составу растворителя, потерявшего часть воды за счет гидратации индифферентного электролита, изменяются пропорционально 1 / е, что подтверждает вывод о преимущественной гидратации в рассматриваемой системе. [11]
Значения констант образования комплексов, приведенные в табл. 11 - 2, несколько неточны, поскольку наряду с реакцией между металлом и ЭДТА имеют место конкурирующие взаимодействия Y4 - с протонами и ионов металла с другими частицами, находящимися в растворе. Как указывал Рингбом [4], большей частью нет необходимости знать концентрацию каждого вида частиц в растворе; гораздо более важна степень полноты интересующей реакции. [12]
Знание констант образования комплексов Ki позволяет характеризовать состояние комплексных частиц в растворе в зависимости от концентрации ионов металла и лигандов. [13]
Сравнивая константу образования комплекса уранила с соответствующими константами бипротонированных комплексов редкоземельных элементов, величины которых изменяются от 5 5 до 7 5, можно видеть, что большая ковалентность связи в комплексе уранила с избытком компенсирует лишний положительный заряд на ионе редкоземельного элемента. [14]
Страницы: 1 2 3 4