Константа - образование - комплекс
Cтраница 2
Сравнивая константу образования комплекса уранила с соответствующими константами редкоземельных элементов, которые изменяются от 5 5 до 7 5, можно видеть, что большая ковалентность связи в комплексе уранила с избытком компенсирует избыточный положительный заряд на ионе последнего. [16]
Сравнивая константу образования комплекса уранила с соответствующими константами бипротонированных комплексов редкоземельных элементов, величины которых изменяются от 5 5 до 7 5, можно видеть, что большая ковалентность связи в комплексе уранила с избытком комненсирует лишний положительный заряд на ионе редкоземельного элемента. [17]
С использованием констант образования комплексов были рассчитаны кривые растворимости СиО в растворах МЭА разной концентрации. [18]
При анализе констант образования комплексов серебра с этими соединениями при разных температурах ( табл. 6) [134] была найдена хорошая линейная зависимость между логарифмами этих констант и константами ат - и сгр - Гамметта. [19]
Сведения о константах образования комплексов такого состава в литературе отсутствуют. [20]
Уоллес [14] определял константы образования комплексов уранил-иона с сульфатом, используя в качестве метки уран-233. [21]
В большинстве случаев константы образования комплексов величины незначительные, что свидетельствует о небольшой устойчивости этих комплексов. Комплексы могут образовываться только при довольно высоких концентрациях гидротропных веществ. [22]
Таким образом, константу образования комплекса мы выразили через величины, которые можно определить экспериментально. Величину Л получают измерением распределения вещества В между обоими чистыми растворителями. Затем измеряют общую концентрацию вещества В в обеих фазах при различных общих концентрациях вещества А. СА константа образования остается постоянной. [23]
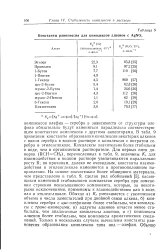 |
Константы равновесия для комплексов алкенов с AgNO3. [24] |
В табл. 9 приведены константы образования комплексов некоторых алкенов с ионом серебра в водном растворе и комплексов с нитратом серебра в этиленгликоле. Комплексы значительно более стабильны в воде, чем в органическом растворителе. Для первых пяти доноров ( RCH CH2), перечисленных в табл. 9, величины Кс для взаимодействия в водном растворе увеличиваются параллельно росту R; по причинам, далеко не очевидным, константы взаимодействия в этиленгликоле изменяются в противоположном направлении. На основе значительно более обширного материала, чем представлено в табл. 9, сделан ряд обобщений [5], касающихся изменений стабильности комплексов серебра при изменении строения ненасыщенного компонента, которые, за некоторыми исключениями, применимы к взаимодействиям или в воде, или в этиленгликоле. Обычно а) / Сс уменьшается с увеличением объема и числа заместителей при двойной связи алкена, б) комплексы серебра с ис-олефинами более стабильны, чем комплексы с транс-изомерами; в) аддукты алкинов отчасти менее стабильны, чем аналогичные комплексы алкенов, и г) комплексы алкенов более стабильны, чем комплексы ароматических соединений. [25]
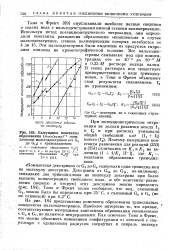 |
Кажущиеся константы образования ( моль / литр 1 комплексов мальтодекстринов ( от Gt. [26] |
На рис. 184 представлены константы образования трииодидных комплексов мальтодекстринов. Наиболее интересно то, что кривые, соответствующие кажущимся константам образования комплексов с Ge и G7, не являются непрерывными. [27]
Подтверждение вывода об уменьшении констант образования комплексов Rh ( PPh3) 2 ( олефин) С. [28]
При определении состава и констант образования комплексов органических веществ в растворах обычно коэффициенты активности всех веществ, участвующих в образовании комплексов, принимают равными единице. [29]
 |
Кривые сила тока - напряжение Cd2 с нитрилуксусной кислотой, полученные с помощью ртутного. [30] |
Страницы: 1 2 3 4