Константа - первый порядок
Cтраница 1
Константа первого порядка была измерена по наклону зависимости логарифма оптической плотности от времени, представленной на рис. 7.3. Кривую уменьшения оптической плотности снимали при значении тока до 100 ма. [1]
 |
Зависимость периода полураспада диэтилового эфира от начального давления.| Константа скорости мономолекулярной реакции в. [2] |
Следовательно, и константа первого порядка и время превращения определенной доли вещества должны зависеть от концентрации ( или давления) А. [3]
Радикальная реакция характеризуется константой первого порядка и энергией активации 33.5 ккал, ионная реакция имеет порядок 3 / 2 и энергию активации 26 0 ккал. [4]
Если плоская поверхность подвергается воздействию растворенного вещества по этому механизму, то константа первого порядка, определяющая скорость исчезновения субстрата, должна быть прямо пропорциональной коэффициенту диффузии и обратно пропорциональной квадрату расстояния от границы раствора до поверхности твердого вещества. Величина kL не должна зависеть от площади поверхности, на которой происходит реакция. [5]
 |
Некоторые реакции, считающиеся мономолекулярными. [6] |
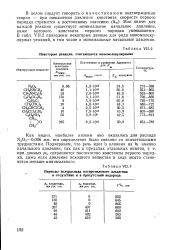
Или иначе: для каждой реакции существует минимальное начальное давление, ниже которого константа первого порядка уменьшается. В табл. VII.2 приведены некоторые данные для ряда мономолекулярных реакций, в том числе и минимальные начальные давления. [7]
 |
Некоторые реакции, считающиеся мономолекулярными. [8] |
Или иначе: для каждой реакции существует минимальное начальное давление, ниже которого константа первого порядка уменьшается. В табл. 18 приведены некоторые данные для ряда мономолекулярных реакций, в том числе и минимальные начальные давления. Как видно, наиболее низким оно оказалось для распада пятиокиси азота ( 0 006 мм); его определение было связано со значительными трудностями. Здесь возникает вопрос о роли продуктов реакции и добавок посторонних инертных газов. Подобное же компенсирующее свойство обнаруживают и другие вещества. Как видно из табл. 19, при высоком давлении альдегида добавки водорода на ход реакции существенно не влияют, но при низком его давлении уменьшают период полураспада до нормального значения, равного приблизительно 600 сек. Таким своеобразным катализатором или, вернее, передатчиком энергии может быть не только водород. [9]
Таким образом, у нас уже имеются данные, необходимые для расчета изменений константы первого порядка ( V / tCb ]) в зависимости от содержания в смеси хлористого водорода. Тем не менее в рамках принятой гипотезы невозможно воспроизвести экспериментальную кривую со значением, полученным для константы ассоциации ( прерывистая линия), или даже исходя из другой величины. [10]
Альтернативный подход к этой проблеме предложен Джорджем [36], который показал, что наблюдавшаяся Бруксом константа первого порядка & абл. Однако с точки зрения кинетики возникает противоречие, так как пропорциональность константы скорости произведению [ НЬ ] [ НЬО2 ] должна вытекать из реакции, имеющей второй порядок по неокисленному гемоглобину, а не первый порядок, как это было точно установлена Бруксом. [11]
Однако это уравнение тождественно уравнению ( 4), отвечающему реакциям первого порядка, с той лишь разницей, что вместо константы первого порядка из уравнения ( 4) здесь фигурирует произведение двух констант. Таким образом, реакция кажется мономолекулярной, или пеевдомономолекулярной. [12]
Однако это уравнение тождественно уравнению ( 4), отвечающему реакциям первого порядка, с той лишь разницей, что вместо константы первого порядка из уравнения ( 4) здесь фигурирует произведение двух констант. Таким образом, реакция кажется мономолекулярной, или псевдомономолекулярной. [13]
Путем интегрирования и применения условия стационарности удается получить довольно сложные выражения [55], которые описывают результаты отдельного кинетического опыта в виде кинетической кривой для реакции первого порядка, причем константа первого порядка представляет собой произведение бимолекулярной константы на исходную концентрацию. [14]
Несмотря на некоторые попытки, в особенности Пигмэна ( Pigman, 1944), обобщить данные о влиянии структуры аглюкона на скорость энзиматического гидролиза [ 3-глюкозидов, значительная часть этих данных не укладывается в какую-либо простую схему. Низкая величина константы первого порядка могла бы быть обусловлена несколькими факторами-малым сродством к; энзиму, высокой устойчивостью комплекса энзим-субстрат или сильным ингиби-рованием продуктами реакции. Который из этих факторов в каждом данном случае является главным, может быть установлено лишь путем более полного кинетического исследования, а не посредством простого определения одних констант первого порядка, которое может привести к неправильным выводам. [15]
Страницы: 1 2 3