Константа - равновесие - комплекс
Cтраница 1
Константы равновесия динитропропенидных комплексов указывают на образование соответствующих тринитроциклогексадиенатных комплексов. [1]
При рассмотрении констант равновесия комплексов ионов металлов интересно сравнить константы равновесия для различных лигандов. Ионы двух различных металлов могут иметь одинаковые константы равновесия при образовании комплекса с данным лигандом, но сами скорости реакций могут при этом быть существенно различными, так как равенство констант равновесия означает лишь равенство отношения скоростей. Можно было бы предположить, что скорость образования комплексов Mg и Са лимитируется скоростью разрушения внутренней гидратной оболочки иона металла. Так как разрушение гидратной оболочки Mg происходит приблизительно в 100 раз медленнее, чем гидратной оболочки Са, казалось бы, что разница в скоростях образования комплексов Mg и Са с АТФ может быть связана с общими закономерностями, вытекающими из их взаимодействия с водой. Однако образование комплексов в обоих случаях происходит так быстро, что необходимо искать какое-то другое объяснение. Благодаря своим меньшим размерам Mg имеет более высокую концентрацию заряда, чем Са, и обладает большей эффективностью в отношении поляризации лабильных связей, приводящей к распаду комплекса. Возможно, что вакантные места в координационной оболочке Mg заполняет вода, которая может играть важную роль в реакциях гидролиза. [2]
Ошибки в величинах констант равновесия комплексов ЗЗе и 19а не учтены. [3]
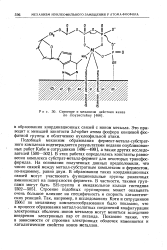 |
Строение и механизм действия киназ по Лоуэнстейну. [4] |
В этих работах определялись константы равновесия комплекса субстрат-металл-фермент для некоторых трансфос-форилаз. На основании полученных данных предположили, что число связей между металл-субстратным комплексом и ферментом, по-видимому, равно двум. В образовании таких координационных связей могут участвовать функциональные группы различных аминокислот на поверхности фермента. Строение подобных группировок может оказывать очень большое влияние на специфичность и скорость каталитических реакций. Так, например, в исследованиях Коти и сотрудников [506] по механизму комплексообразования было показано, что в процессе образования металл-хелатных соединений конфигурации электронных оболочек Ионов металлов могут меняться вследствие внедрения электронных пар от лиганда. Показано также, что в зависимости от строения электронных оболочек изменяются и каталитические свойства ионов металлов. [5]
Тот факт, что константы равновесия комплексов циркония ( гафния) с молочной, винной и яблочной кислотами мало различаются, указывает на наличие одинакового механизма комплексообразования циркония ( гафния) с указанными оксикислотами. [6]
Как видно из табл. 2, константа равновесия комплекса К ( тик т шп и свободная энергия & FC) существенно изменяется при переходе от неполнрвого растворитеса к полярному. [7]
Этот метод использован [25] для расчета констант равновесия комплексов, образующихся между хлоридом олова и некоторыми циклическими эфирами в бензоле. Речь идет о комплексных соединениях типа АВ2, где А - хлорид олова, а В - основание. Если точке эквивалентности реакции соответствует объем AF, то степень диссоциации комплекса аАВ / АС. [9]
В настоящей работе предлагается методом Бенеши - Гильдебранда определить константу равновесия комплекса йод - бензол в ССЦ. [10]
Используются и другие методы определения энергии ВС, основанные на спектроскопическом изучении температурной зависимости константы равновесия комплексов. [11]
Понижение ионизационного потенциала донора сопровождается не только смещением полосы поглощения в длинноволновую область, но и возрастанием констант равновесия комплексов в растворах. В этом случае следует ожидать также повышения интенсивности полосы поглощения переноса заряда. В некоторых растворах увеличение коэффициента поглощения сопровождается не возрастанием, а уменьшением константы равновесия комплексов. В этом случае система существует только в момент соударения донора и акцептора, поэтому ассоциация не обнаруживается обычными химическими методами. [12]
Использование карбонилродий-3 - фторацетилкамфо-рата в качестве активного компонента НЖФ имеет по сравнению с использованием для тех же целей солей серебра следующие преимущества: 1) более сильное взаимодействие с разделяемыми соединениями, позволяющее получить лучшее отделение предельных углеводородов от непредельных; 2) влияние структуры олефина на константу равновесия комплекса более выражено, 3) комплексы родия растворимы в неполярных фазах, на которых хорошо разделяются и предельные соединения. [13]
Константы равновесия реакции комплексообразования были определены в интервале температур 10 - 40 по уравнению Бенеши-Гильдебранда. Константа равновесия комплексов возрастает с увеличением энергии сродства к электрону акцептора, с уменьшением потенциала ионизации донора и с понижением температуры реакции комплексообразования. [14]
Найдены константы равновесия комплексов и подсчитаны концентрации мономеров, димеров, тримеров, тетрамеров, пентамеров и гекса-меров. Комплексы триоксаяа с дихлорэтаном отсутствуют. [15]
Страницы: 1 2