Константа - равновесие - комплекс
Cтраница 2
Оказалось, что в случае электрондонорного заместителя X ( - С2Н5) образование комплекса идет за счет замещенного ядра, в случае электронакцепторного ( СН3СО, CN) - за счет незамещенного. Различие в константах равновесия комплексов в последнем случае доказывает участие замещенного ядра в комплексообразовании, которое авторы рассматривают как трансаннулярный эффект с лежащим в его основе индуктивным влиянием. Нужно полагать, что здесь имеет место внутримолекулярный комплекс с переносом заряда между двумя бензольными кольцами. [16]
Нужно отметить, что состав элюирующего раствора определяется только концентрациями всех ионов в регенерате. Уравнения, которые составляются из этих переменных величин, содержат константы равновесия отдельных редкоземельных цит-ратных комплексов, причем эти константы для каждого элемента несколько различны. Поэтому концентрация Cit3 - и рН в равновесии с каждым редкоземельным элементом в развивающихся полосах будут немного различны, а это создает возможность к разделению полос. Например, если ион неодима находится в полосе празеодима, то он вступит в контакт с цитрат-ионами ( СН3 -), которые способствуют его переходу в раствор, и будет продвигаться вперед быстрее, чем ионы празеодима. [17]
Этот процесс наиболее вероятен при образовании слабых комплексов донорно-акцепторного типа. Изучение интенсивности такой полосы дает возможность определить состав и оценить константу равновесия комплекса. [18]
Комплексы циркония более устойчивы, чем соответствующие комплексы гафния. Из дикарбоновых кислот наиболее прочные соединения с цирконием и гафнием образует щавелевая кислота. Константы равновесия комплексов циркония и гафния с оксикис-лотами уменьшаются в следующем ряду кислот: триоксиглутаровая лимонная винная молочная - яблочная. Нарушение этого правила наблюдается только в одном случае: К для лактата гафния больше, чем К. [19]
Такое сте-рическое сжатие отсутствует в основном состоянии 1 3 - ДНБ, и поэтому уменьшается движущая сила комплексообразования. Для 1 1-диметокси - 2 4 б-тринитроциклогексадиенатного комплекса ( 19а) константа равновесия была определена несколькими исследователями [24, 92, 106, 205, 210]; ее значение колеблется от 2 103 до 20 103 л / моль в зависимости от условий опыта. При сравнении констант равновесия комплексов 19а и ЗЗе становится очевидным, что увеличение стабильности анионного а-комплекса происходит за счет нитрогруппы, расположенной в пара-положении к тетра-эдрическому углеродному атому кольца. Такой же порядок величины предсказан методом СМ [23] ( разд. III) и эмпирическим методом Миллера ( разд. Отсюда следует, что п-нитрогруппа приблизительно в 3 раза более эффективна в стабилизации, чем о-нитрогруппа. [20]
Деполяризация флуоресценции малой молекулы, обладающей в жидком растворе коротким временем вращательной релаксации, сильно снижается, если эту молекулу связать с большой молекулой полимера. Таким способом Велик [310] измерил константы равновесия комплексов коферментов, а Лоуренс [311] изучил равновесие между красителями и белками и их комплексами. [21]
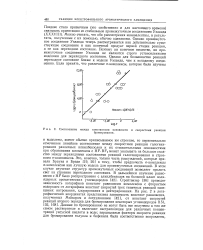 |
Соотношение между константами основности и скоростями реакции. [22] |
Это, конечно, только часть рассуждений, которые привели Брауна и Брэди [19, 20] к тому, чтобы предпочесть сг-комплексы я-комплексам как лучшую модель для промежуточных соединений. В этом случае изучение структур промежуточных соединений позволяет пролить свет на строение переходного состояния. Стрейтвизер [36] приводит зависимость логарифмов констант равновесия комплексов с фтористым водородом от логарифмов констант скоростей трех типичных реакций замещения: нитрования, хлорирования и дейтерирования. [23]
В определенных системах возможно найти также константы скоростей и константу равновесия в процессах комплексообразо-вания. Химический сдвиг, например, может быть использован для определения констант равновесия комплексов с переносом заряда. [24]
Понижение ионизационного потенциала донора сопровождается не только смещением полосы поглощения в длинноволновую область, но и возрастанием констант равновесия комплексов в растворах. В этом случае следует ожидать также повышения интенсивности полосы поглощения переноса заряда. В некоторых растворах увеличение коэффициента поглощения сопровождается не возрастанием, а уменьшением константы равновесия комплексов. В этом случае система существует только в момент соударения донора и акцептора, поэтому ассоциация не обнаруживается обычными химическими методами. [25]
Замещение водорода у двойной связи приводит к резкому уменьшению взаимодействия олефинов с родием. Тризамещенные алкены характеризуются весьма небольшим взаимодействием с комплексами родия, а тетразамещениые олефины ( например, 2 3-диметилбутен - 2) вообще не взаимодействуют с родием. Как и в случае комплексов с серебром, ис-изомеры олефинов реагируют более сильно с комплексом родия, чем транс-изомеры. Константы равновесия олефииов с комплексом родия для ряда н-олефинов RCH CH2 не зависят от длины цепи R, в то время, как в случае комплексов с серебром эта величина уменьшается с ростом радикала. В монозамещенных олефи-нах в а-положешш наблюдается для обоих типов комплексов небольшое уменьшение константы, однако если в а-положении имеется два заместителя, то наблюдается резкое уменьшение константы равновесия комплекса. Так, отношение констант комплексообразования для 3 3-диметилбутена - 1 и бутена-1 составляет Vs9 для родия и только 7з для серебра. Замещение в р-положении ( например, для 4-метшшентена - 1) практически не влияет на константу комплексообразования с родием и заметно влияет на константу комплексообразования с серебром. [26]
Страницы: 1 2