Константа - равновесие - реакция - диссоциация
Cтраница 1
Константы равновесия реакций диссоциации ( выраженные в атмосферах) стремятся к очень большим значениям при возрастании температуры, в то время как для реакций с сохранением числа частиц ( например, реакции продолжения цепей в системе водород - кислород) константы равновесия приближаются к единице. В сочетании с очень высокими концентрациями активных центров, которые накапливаются в процессе нестационарного разветвления, это приводит к тому, что стадии продолжения цепей оказывают гораздо большее влияние на течение всей цепной реакции, чем при низких температурах или в квазистационарных условиях. [1]
Константа равновесия реакции диссоциации называется константой диссоциации вещества МА. Константы диссоциации кислот или гидроксидов являются характеристикой силы этих соединений. [2]
Чему равна константа равновесия реакции диссоциации HI при той же температуре. [3]
Для нейтральных газов приводятся константы равновесия реакций диссоциации на одноатомные газы, для ионизованных положительно заряженных газов - константы равновесия реакций ионизации соответствующего нейтрального газа, для отрицательно заряженных газов - константы равновесия реакции отрыва электрона. [4]
Поскольку в таблицах приводятся константы равновесия реакций диссоциации двух - и многоатомных газов на атомы ( или ионы), а точность вычисленных значений термодинамических функций одноатомных газов примерно на порядок выше, чем у двух - и многоатомных газов, погрешность величины изменения Ф - потенциала в реакции диссоциации ( ДФу) практически равна погрешности величины Ф соответствующего диссоциирующего газа. [5]
В приведенных восьми уравнениях констант равновесия реакций диссоциации содержится 11 неизвестных парциальных давлений газов, составляющих продукты сгорания, неизвестна температура, величина которой определяет значение констант равновесия. [6]
Таким образом, данные Бребрика по константе равновесия реакции диссоциации ZnTe следует считать, очевидно, наиболее надежными. [7]
На основании найденных в работах [1358, 1359, 1745] значений констант равновесия реакции диссоциации р2 авторами Справочника были вычислены значения Do ( Ра) 36 7 и 32 ккал / моль соответственно. [8]
Основной термодинамической характеристикой комплекса МАп в растворе является константа равновесия реакции диссоциации на центральный ион М и адденд А. [9]
Теплота диссоциации может быть вычислена на основании измерений констант равновесия реакции диссоциации двумя методами. [10]
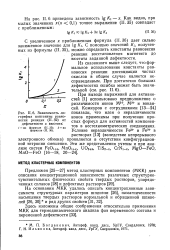 |
Зависимость логарифма константы равновесия реакции ( И. 32 от дефектности х вюстита. [11] |
Из сказанного выше следует, что формальное использование константы равновесия реакции диссоциации чистых окислов в общем случае является несправедливым. [12]
Прейнер и Брокмеллер [3317] и Сток, Гибсон и Стамм [3866] измерили константу равновесия реакции диссоциации: Р4 ( газ) 2Р2 ( газ) в интервале температур 1100 - 1500 К. По этим данным авторы Справочника вычислили D0 ( P4 - 2Р2) 53 62 0 05 ккал / моль. Выполненное Дровартом и Гольдфингером [1407] масс-спектрометрическое исследование равновесий в парах фосфора привело к величине D298 ( P4 - 2Р2) 55 7 0 5 ккал / моль, или D0 ( P4 - 2Р2) 54 0 ккал / моль. Эта величина хорошо согласуется с вычисленной по данным Стока и др. [3866], но менее точна. [13]
Для определения теплоты диссоциации по уравнению ( 9) необходимы данные о константе равновесия реакции диссоциации в некотором интервале температур. [14]
Следовательно, для определения скорости окисления окиси азота необходимо знать значение константы скорости прямой реакции и значение константы равновесия реакции диссоциации двуокиси азота. [15]
Страницы: 1 2 3