Константа - равновесие - реакция - диссоциация
Cтраница 2
В табл. 10 приведены величины энергий разрыва связи в различных соединениях, вычисленных на основании оптических данных и результатов измерений констант равновесия реакций диссоциации. [16]
Использование констант равновесия указанных реакций во многих случаях является более предпочтительным, чем констант, приведенных в основных таблицах II тома, но для расчета химических равновесий вопрос о выборе тех или иных элементарных реакций не принципиален, поскольку константа равновесия любой реакции может быть легко вычислена через константы равновесия реакций диссоциации на атомы. [17]
В уравнения ( 4) и ( 5) Рс2НС РСЗНЯ - парциальные давления этана и пропана; роУ, роУъ - парциальные давления метил - и этил-радикалов; х - часть распавшегося алкана; Ь, &2, & з, &4, &5, Кр - соответственно константы скорости первичного распада СгН6 и СзНз на радикалы, реакций замещения метальных и зтильных радикалов с молекулами пропана, реакции атомов Н с молекулами этана, реакции рекомбинации этильных радикалов и константы равновесий реакций диссоциации этильных и изопропильных радикалов на олефин и атомарный водород; и - относительная концентрация добавки этилена или пропилена. [18]
Если рассмотреть распад сложных молекул, то значения констант равновесия указывают на наибольшую вероятность процессов симметричного распада. Константы равновесия реакций диссоциации алканов на радикалы, как известно, определяют равновесные концентрации радикалов в зоне реакции. [19]
Чему равна константа равновесия реакции диссоциации при 450 С. [20]
Термодинамические функции рассчитаны с использованием отнесений колебаний по Шеппарду [1344], средних длин связей, рекомендованных Саттоном [1449], и оценочного значения барьера внутреннего вращения 4 0 ккал / молъ. Эти функции в сочетании с константами равновесия реакции диссоциации до пропилена и йодистого водорода при 511 7 К, приводимыми в работе Бозе и Бенсона [149], дают АЯ / 98 ( g) - 10 5 ккал / молъ. [21]
Термодинамические функции рассчитаны с использованием отнесений колебаний по Шеппарду [1344], средних длин связей, рекомендованных Саттоном [1449], и оценочного значения барьера внутреннего вращения 4 0 ккал / молъ. Эти функции в сочетании с константами равновесия реакции диссоциации до пропилена и йодистого водорода при 511 7 К, приводимыми в работе Бозе и Бенсона [149], дают AHf2ss ( g) - 10 5 ккал / молъ. [22]
 |
Изменение стандартной энтальпии сублимации элементных веществ в пределах IV группы. [23] |
MnOj ( - 466), Мп2Оэ ( - 878), МпзО4 ( - 1280), но константы равновесия реакций диссоциации оксидов на простые вещества в этом ряду соответствуют выражениям, в которых давление кислорода возводится в различную степень. Отнесение Дс к 1 моль кислорода также не может служить характеристикой стабильности соединений, так как эти оксиды ( кроме МпО) диссоциируют не на Мп и 02, а на соответствующий низший оксид и кислород. [24]
В 1961 г. была опубликована работа Филлипса и Сагдена [ 3236а ] по спектроскопическому изучению фотометрическим методом пламен водородо-кислородо-азотных смесей с малыми добавками йода. Этими авторами были проведены измерения интенсивности полосы 0 - 4 молекулы JO, на основании которых определена температурная зависимость константы равновесия реакции диссоциации JO на атомы. Найденное в работе [ 3236а ] значение Do ( JO), по-видимому, завышено. [25]
Следовательно, для определения температуры сгорания в дополнение к уравнению энергии определяющему общий тепловой эффект необходимо иметь еще ряд уравнений, связывающих между собой температуру и степени диссоциации. Число этих уравнений должно быть равно числу процессов диссоциации. Такими уравнениями являются уравнения для констант равновесия реакций диссоциации. [26]
За последнее время появилось большое число новых ком-плексонов, сложных по составу, содержащих несколько ими-нодиацетатных групп, в молекулы которых входят различные гетероатомы: галогенов, серы, фосфора и других элементов. Изменение состава комплексонов приводит к новым свойствам образующихся комплексных соединений. Основной термодинамической характеристикой комплексных соединений является константа равновесия реакции диссоциации комплекса - константа устойчивости, или, что то же самое, ее обратная величина - константа нестойкости. Эта величина является наиболее объективной термодинамческой характеристикой прочности комплекса. [27]
В вводном разделе к настоящей главе отмечалось, что различие в значениях термодинамических функций соответствующих соединений протия и природного водорода находится за пределами точности определения этих функций. Ввиду этого во II томе Справочника не приводятся отдельные таблицы для двухатомного протия и для природной смеси двухатомного водорода, подобно тому как нет отдельных таблиц для HjO и ШО, ОН1 и ОН, а приводятся таблицы только для На, НаО и ОН. Термодинамические функции протия использованы для вычисления констант равновесия реакций диссоциации HLT, H1DO, НТО и НЧЭ. [28]
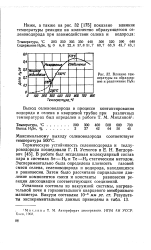 |
Влияние температуры на образование и разложение. [29] |
В работе был исследован молекулярный состав пара в системах Se - Н2 и Те - Н2 статическим методом. Экспериментально была определена плотность газовой смеси селена, селеноводорода и водорода, находящихся в равновесии. Затем было рассчитано парциальное давление компонентов смеси и константы равновесия реакции диссоциации соответствующих соединений. [30]
Страницы: 1 2 3