Константа - равновесие - реакция - комплексообразование
Cтраница 1
Константы равновесия реакции комплексообразования были определены в интервале температур 10 - 40 по уравнению Бенеши-Гильдебранда. Константа равновесия комплексов возрастает с увеличением энергии сродства к электрону акцептора, с уменьшением потенциала ионизации донора и с понижением температуры реакции комплексообразования. [1]
Определены константы равновесия реакций комплексообразования с ацетатом ртути 36 сульфидов, типа содержащихся в нефтях, вычислены равновесные выходы комплексных соединений в интервале 0 - 60 С, а также тепловые эффекты, изобарные потенциалы и энтропии этих реакций. [2]
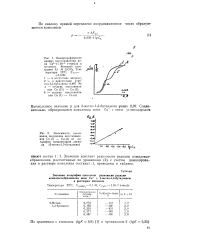 |
Зависимость потенциала полуволны восстановления Си ( I - Си ( о от логарифма концентрации лиганда ( 2-метил - 1 3-бутадиена. [3] |
Значения констант равновесия реакции комплексообразования, рассчитанные по уравнению ( 2) с учетом доминирования в растворе комплекса состава. [4]
Энтальпия образования водородной связи и константа равновесия реакции комплексообразования / СР зависят от растворителя, причем их значения довольно сильно изменяются даже в неполярных растворителях, считавшихся одинаковыми по их способности к сольватации оснований. [5]
На этом основано использование ГЖХ для определения констант равновесия реакций комплексообразования. [6]
Ядимирский и Бударин [123 - 124] предложили способ определения констант равновесия реакций комплексообразования в растворах, основанный на изучении зависимости каталитических полярографических токов от концентрации веществ, образующих комплексное соединение с веществом-катализатором. [7]
По-видимому, такая немонотонная зависимость констант гидролиза и констант равновесия реакций комплексообразования с сульфат-ионами от радиуса обусловлена влиянием строения электронной оболочки катиона на прочность образуемых ими соединений. [8]
Таким образом, любой физико-химический метод, позволяющий определять константы равновесия реакций комплексообразования ( например, с помощью способов, рассмотренных в разд. [9]
Этот универсальный метод точного определения молярных коэффициентов светопоглощения и констант равновесия реакций комплексообразования основан на решении уравнения с двумя неизвестными для двух или более опытов. Метод предполагает знание типа реакции или состава комплекса, установленных независимым путем. [10]
Этот универсальный метод точного определения молярных коэффициентов светопоглощения и констант равновесия реакций комплексообразования основан на решении уравнения сдвумя неизвестными для двух или более опытов. Метод предполагает знание типа реакции или состава комплекса, установленных независимым путем. [11]
Этот универсальный метод точного определения молярных коэффициентов светопоглощения и констант равновесия реакций комплексообразования основан на решении уравнения с двумя неизвестными для двух или более опытов. Метод предполагает знание типа реакции или состава комплекса, установленных независимым путем. [12]
Сложнее обстоит дело с исследованием сильно диссоциирующих комплексов, когда константы равновесия реакций комплексообразования соизмеримы с поправочными множителями. В таких случаях кажущиеся константы равновесия существенно отличаются от истинных. Отсюда следует, что к результатам изучения слабых комплексов с помощью графических приемов, основанных на использовании уравнения (11.12) для кажущейся константы равновесия ( см. разд. Поскольку при этом оба параметра, лгк и Кс, определяются одновременно, неправильное исходное выражение для константы равновесия может заметно исказить величину физического параметра комплекса. [13]
Определение термодинамических функций по изобаре химической реакции сводится к определению констант равновесия реакций комплексообразования или коэффициентов распределения ( Я) при нескольких температурах. [14]
Необходимо отметить, что константы устойчивости могут располагаться в ином порядке, чем константы равновесия реакций комплексообразования циркония и гафния с оксикислотами. [15]
Страницы: 1 2