Константа - равновесие - реакция - комплексообразование
Cтраница 2
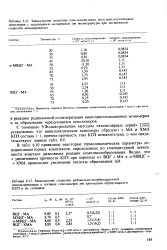
В табл. 6.10 приведены некоторые термодинамические параметры до-норно-акцепторных комплексов, определенные по температурной зависимости констант равновесия реакции комплексообразования. Видно, что с увеличением прочности КПЗ при переходе от ВЦГ МА к ос - МВЦГ ХМА происходит увеличение теплоты образования АН. [17]
Установлены оптимальные условия его образования. По кривым оптическая плотность - рН вычислены молярные коэффициенты погашения, константа равновесия реакции комплексообразования и константа устойчивости. Высказано предположение, что в образовании соединения принимает участие родий ( III) в катионной форме. [18]
Для сходных ионов с равным числом зарядов при отсутствии комплексообразования отношение коэффициентов распределения может быть весьма близким к единице. При этом хроматографиче-ское разделение ионов в равновесных условиях оказывается невозможным или, по крайней мере, очень трудным. Часто константы равновесия реакций комплексообразования для сходных ионов различаются между собой больше, чем коэффициенты распределения простых ( некомплексных) ионов. Следовательно, в этих случаях для улучшения разделения могут быть использованы комплексо-образователи. [19]
Данных о прочности комплексных соединений ионов-катализаторов с теми или иными лигандами недостаточно для оценки маскирующего действия комплексообразователей, необходимы также сведения о каталитической активности образующихся комплексов. Для маскирования мешающих ионов представляют интерес лишь каталитически неактивные комплексы этих ионов. Поэтому ценность констант равновесия реакций комплексообразования, полученных кинетическим методом, несомненна. [20]
Для близких химически ионов с равным числом зарядов при отсутствии комплексообразования отношение коэффициентов распределения ионов между твердой фазой ионита и раствором близко к единице. Это делает трудным разделение ионов в равновесных условиях. Комплексообразование позволяет решить этот вопрос, так как константы равновесия реакций комплексообразования для близких по свойствам ионов различаются более резко, чем коэффициенты распределения простых, некомплексных ионов. [21]
Качественные теории комплексообразования позволяют ориентироваться в большом экспериментальном материале по химии комплексообразования. Как и отмечалось выше, количественных теоретически обоснованных подходов, которые позволяли бы априори оценивать константы устойчивости комплексов металлов, пока не существует. Задача создания таких методов очень сложна и далека от своего решения. В то же время накоплен большой массив данных по константам равновесий реакций комплексообразования. [22]
Весь арсенал методов, которыми располагает современная наука для исследования строения молекул и природы химической связи, в принципе применим для изучения молекулярных комплексов. Исследование молекулярных комплексов, выделенных в чистом виде и находящихся в твердом или жидком состоянии, принципиально ничем не отличается от исследования любых других индивидуальных соединений. В таких случаях экспериментально измеряемые физико-химические свойства систем характеризуют не индивидуальный комплекс, а относятся к равновесной смеси комплекса с исходными компонентами. Для получения данных, относящихся к комплексу, необходимо знать константу равновесия реакции комплексообразования и соответствующие параметры исходных молекул. [23]
Растворы соединения реагента с W ( VI) имеют максимум свето-поглощения при 420 - 430 нм, в растворах 100 % - ной H2S04 максимум гипсохромно смещается к 410 нм. Для количественного образования соединения вводят - 4000-кратный избыток пирокатехина. В растворе образуются два соединения с молярным соотношением W: R 1: 1 и 1: 2; последнее соединение преобладает. В растворах 97 % - ной H2S04 молярный коэффициент погашения составляет 5 2 - 103 ( 420 нм), константы равновесия реакций комплексообразования равны ( 0 6 - 2 1) - 10 - 1 ц ( 1 1 - 1 7) - 10 для соединения с соотношением компонентов 1: 1 и 1: 2 соответственно. [24]
Растворы соединения W ( VI) с гидрохиноном имеют максимум светопоглощения при 470 - 480 нм. При увеличении концентрации H2S04 до 100 % он гипсохромно смещается, кривая светопоглощения имеет максимум при 450 нм. Окраска развивается 2 часа, а затем постоянна; рекомендуется вводить - 1500-кратный избыток гидрохинона. При взаимодействии с гидрохиноном образуется два соединения с отношением W: R - 1: 1и1: 2, в растворах с концентрацией H2S04 97 % преобладает второй комплекс. В растворах 97 % - ной H2S04 молярный коэффициент погашения равен 6 7 - 103 ( 470 нм), константа равновесия реакций комплексообразования ( 2 0 - 7 4) - 10 - - 2 и ( 1 4 - 1 9) - 10 - 5 для соединений с соотношением компонентов 1: 1 и 1: 2 соответственно. При анализе сталей содержащих Mn, Ni, Co, Mo, Cr, V, Cu, Ti [555], Fe ( III) nMo ( VI), мешающие определению, восстанавливают хлоридом олова ( П) в среде Н3Р04 для предотвращения восстановления вольфрама. [25]
Страницы: 1 2