Константа - реакция
Cтраница 2
Поэтому константа реакции находится в тесной связи с механизмом реакции, о типе которого можно заключить по ее знаку ( см. пример на стр. [16]
Здесь константа реакции р отрицательна, поэтому реакция тем более облегчается, чем выше электронная плотность в реакционном центре. Согласно (6.23), увеличение электронной плотности на карбонильной группе повышает основность карбонильного кислорода; поэтому он легче подвергается электрофмль-ной атаке протоном и, следовательно, с большей легкостью может отщепляться в виде воды. Присоединение основания к карбонильной группе, активированной ( - заместителем, из-за высокой скорости процесса уже не оказывает существенного влияния на кинетику реакции в целом. [17]
Дана константа реакции Cu ( I) ( тв. [18]
Для константы бариевой реакции при t 18 С вычисляются следующие значения. [19]
Значение константы реакции р для данной серии в определенных условиях постоянно, независимо от положения заместителей ( мета - или пара) в реагирующем соединении. [20]
Величина константы реакции р является мерой восприимчивости реакции к влиянию заместителей. Если допустить, что основное стабилизующее действие заместителя сводится к дело-кализации заряда ( разд. То, что значения р для большинства образующих карбониевый ион реакций в растворах значительно меньше ( например, р - 4 54 для грег-кумилхлорида), подразумевает, что плотность заряда в сольватированном переходном состоянии такой реакции значительно меньше, чем в свободном газообразном ионе. [21]
Величина константы реакции ря при полярографическом восстановлении почти всегда положительна, что делает эту константу практически бесполезной для выяснения механизмов реакций. Положительная величина ря только подтверждает в настоящее время уже несомненный факт, что электрон является нуклеофильным реагентом. [22]
Из констант реакций р-арилэтильных соединений можно получить ценные сведения о степени р - депротонирования в переходном состоянии. [23]
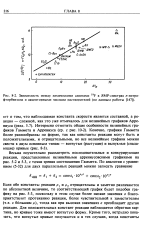 |
Зависимость между химическими сдвигами 19F в ЯМР-спектрах л-нитро-фторбензола и акцепторными числами растворителей ( по данным работы. [24] |
Если обе константы реакции pl и р2 отрицательны и заметно различаются по абсолютной величине, то соответствующий график будет подобен графику на рис. 5 - 3, поскольку в этом случае более низкие значения о благоприятствуют протеканию реакции, более чувствительной к заместителям ( т.е. с большим р), тогда как при высоких значениях о преобладает другая реакция. Для положительных констант реакции наблюдается обратная картина, но кривые тоже имеют вогнутую форму. [25]
Кр - константа реакции при pconst; Kv - констаята реак-дии при Vconst; индекс указывает на стандартное состояние. Для индивидуальных твердых F жидких веществ в качестве стандартного состояния принимают состояние их при данной температуре при давлении 1 атм. За стандартное состояние индивидуального газа принимается состояние гипотетического идеального газа / фугитивность которого равна единице при данной температуре. Свойства реальных газов при давлении 1 атм незначительно отличаются от свойств газов в стандартном состоянии, и при технологических расчетах этой разницей можно v пренебречь. Рассматривая протекание газовой реакции в стандартных условиях, следует иметь в виду, что парциальное давление каждого из компонентов реакции равно 1 атм. Применительно к растворам в качестве стандартного состояния испбль-зуют, как правило, либо стандартное состояние чистого вещества, либо стандартное состояние гипотетического 1 М раствора со свойствами бесконечно разбавленного раствора. [26]
Кр - константа реакции при pconsi, Kv - константа реак-дии при V const, индекс указывает на стандартное состояние Для индивидуальных твердых F жидких веществ в качестве стандартного состояния принимают состояние их при данной температуре при давлении 1 атм За стандартное состояние индивидуального газа принимается состояние гипотетического идеального газа, фугитивность которого равна единице при данной температуре Свойства реальных газов при давлении 1 атм незначительно отличаются от свойств i азов в стандартном состоянии, и при техноло. [27]
К - константа реакции; cs и Cs - концентрации соответственно газовой фазы и твердого вещества на поверхности раздела, выраженные в молях. [28]
По условию константа реакции диссоциации мета - или пара-замещенных бензойных кислот в воде при 25 С приравнивается единице. [29]
Поскольку знак константы реакции тесно связан с ее механизмом ( см, гл. [30]
Страницы: 1 2 3 4