Константа - скорость - диссоциация
Cтраница 1
Константы скорости диссоциации и рекомбинации можно определять и в том случае, если соответствующая слабая кислота не восстанавливается, однако дает предельные токи разряда ионов водорода, определяемые скоростью диссоциации кислоты. Единственный пока случай такого рода обнаружил Кута [56], исследуя полярографическое поведение борной кислоты. [1]
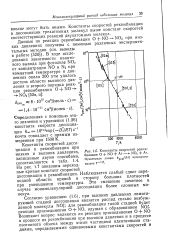 |
Константы скоростей рекомбинации О N0 Аг - NO2 Аг. Пунктирная линия. пекД пропорциональна Т 1 - 9. [2] |
Константы скоростей диссоциации и рекомбинации при низких и высоких давлениях, записанные двумя способами, сопоставляются в табл. 1.4. На рис. 1.7 показаны переходные кривые констант скоростей диссоциации и рекомбинации. Наблюдается слабый сдвиг переходной области кривой в сторону больших плотностей при уменьшении температуры. [3]
Константы скорости диссоциации и рекомбинации можно определять и в том случае, если соответствующая слабая кислота не восстанавливается, однако дает предельные токи разряда ионов водорода, определяемые скоростью диссоциации кислоты. Единственный пока случай такого рода обнаружил Кута [56], исследуя полярографическое поведение борной кислоты. [4]
Константы скорости диссоциации молекул в других газах принято относить к аргону и характеризовать числом, показывающим, во сколько раз / с в рассматриваемой среде отличается от k в аргоне при той же температуре. Такие числа, как правило, слабо зависят от температурного интервала измерений, исключая очень низкие температуры, при которых kJ сравнимо с энергией ван-дер-ваальсового притяжения сталкивающихся частиц, и очень высокие температуры ( б 10), при которых эффективность столкновений определяется в основном геометрической формой молекулы среды и числом входящих в нее атомов. [5]
 |
Константы скорости образования и диссоциации ионных пар ( 25 С. [6] |
Константы скорости диссоциации SSIP обычно не более чем в десять раз отличаются от величин для диффузионно-контролируемых реакций. [7]
Константы скоростей диссоциации других молекул сопоставимы с представленной выше. Возможность варьирования молекулярных параметров в гомологических рядах галогенидов щелочных металлов, например плотности энергетических уровней, может иметь большое значение для теорий диссоциации. Однако в настоящее время константы скоростей диссоциации этого класса веществ экспериментально измерены недостаточно точно. [8]
Из константы скорости диссоциации воды на ионы ( & 2 6 - 10 - 5) следует, что энтропия активного комплекса сильно отрицательна. Это указывает на значительную сольватацию в переходном состоянии. [9]
Выражение константы скорости диссоциации ( 1) получено в предположении быстрого обмена колебательными квантами независимо от номера уровня, что, строго говоря, верно только для гармонического осциллятора. Ангармонизм молекулярных колебаний приводит к двум качественным особенностям распределения колебательной энергии в процессе диссоциации. Отличие распределения от больцмановского тем больше, чем больше ангармоничность колебаний, и для верхних уровней оно может быть весьма значительным. Во-вторых, скорость возбуждения ангармонических осцилляторов п - - п 1 при достаточно больших номерах колебательных уровней п отнюдь не мала по сравнению со скоростью обмена квантами. [10]
Величина константы скорости диссоциации очень хорошо совпадает с данными Дэвиса. [11]
Зависимость константы скорости диссоциации от давления р была исследована в ударных волнах [ 52а ] при высоких р и температурах около 1500 К. [12]
Значение константы скорости диссоциации азота в столкновениях N2 - Аг, играющих основную роль в начальной зоне ударной волны, известно [7, 8], поэтому можно с уверенностью рассчитать изменение температуры, плотности, а также концентраций молекул N2 и атомов N за фронтом ударной волны. Далее надо учесть, что заселенность электронного состояния В22 ( Na) ( реакции ( III), ( IV)) приходит в локальное-равновесие с основным состоянием иона за время порядка времени жизни возбужденного состояния, составляющее - 0 04 мк / сек. [13]
Значение константы скорости диссоциации азота в столкновениях N2 - Аг, играющих основную роль в начальной зоне ударной волны, известно [7, 8], поэтому можно с уверенностью рассчитать изменение температуры, плотности, а также концентраций молекул N2 и атомов N за фронтом ударной волны. Далее надо учесть, что заселенность электронного состояния B22 ( Nt) ( реакции ( III), ( IV)) приходит в локальное равновесие с основным состоянием иона за время порядка времени жизни возбужденного состояния, составляющее - 0 04 мк / сек. [14]
Так как константы скорости диссоциации не могут быть измерены непосредственно, для установления их определяют константы скорости таких процессов, которые протекают через стадию диссоциации соединения на свободные радикалы. Применяемые с этой целью реакции должны удовлетворять следующим требованиям: 1) реакции со свободными радикалами должны протекать при низких температурах; 2) применяемые реагенты не должны реагировать с недиссоциированными молекулами органического соединения; 3) применяемые реагенты должны легко определяться количественно. [15]
Страницы: 1 2 3 4