Константа - скорость - образование
Cтраница 3
А-постоянная, зависящая от константы скорости образования зародышей К и растворимости Ср, п - порядок процесса зародыше-образования, Cs - концентрация исходного раствора. Отметим также, что с ростом К и Ср величина А уменьшается. [31]
Из результатов определения отношения констант скоростей образования углекислого газа видно, что продуцирование углекислого газа является результатом вторичной реакции разложения дивинила. [32]
Качественное сопоставление вкладов в константу скорости образования различных изомеров при чисто химическом и радиа-ционно-химическом гидроксилировании нитробензола и анизола ( табл. 6) показывает, что реакции, индуцированные облучением, по своему механизму отличаются от чисто химических. По-видимому, в обычной химии атакующей частицей не является свободный незакомплексованный ОН-радикал. Возможно также, что при химическом гидроксилировании кислород быстро расходуется и механизм гидроксилирования аналогичен таковому для радиаци-онно-индуцированного процесса в растворах, насыщенных закисью азота. [33]
В этой схеме Q - константа скорости образования деполяризатора А, которая может зависеть от концентрации других веществ, участвующих в этой химической реакции. [34]
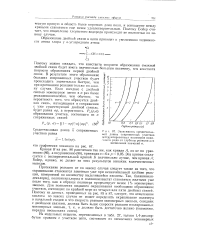 |
Зависимость среднечисло-вой длины сопряженных участков деструктированных полимеров винилового ряда от глубины реакции для нескольких значений а. [35] |
Поэтому можно ожидать, что константа скорости образования смежной двойной связи будет иметь значительно большую величину, чем константа скорости образования первой двойной с связи. В результате этого образование больших сопряженных участков будет происходить значительно быстрее, чем при протекании реакции только по закону случая. [36]
Такое соотношение указывает на различие констант скоростей образования отдельных изомеров. [37]
Такое соотношение указывает на различие констант скорости образования отдельных изомеров. [38]
Для объяснения эффектов существенного уменьшения константы скорости образования молекулярных комплексов с белками по сравнению с диффузйонно-контролируемым пределом и высокой чувствительности процесса к структуре лиганда можно предложить два принципиально различающихся механизма. [40]
Такое соотношение указывает на различие констант скоростей образования отдельных изомеров. [41]
Иными словами, чтобы определить отношение констант скоростей образования двуокиси углерода из бутана и бутадиена, необходимо знать их удельные активности и отношение концентраций, а также удельную активность двуокиси угерода. Все эти данные содержатся в разделе VIII. [42]
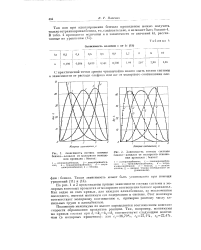 |
Зависимость состава системы бензол-алкилат от молярного отношения пропилен. бензол.| Зависимость состава системы оензол-алкилат от молярного отношения пропилен. бензол. [43] |
Положение максимума по высоте определяется соотношением констант скорости образования продуктов реакции. [44]
Страницы: 1 2 3 4