Константа - скорость - первый порядок
Cтраница 4
В случае диссоциации МО2 переход к константам скоростей первого порядка наблюдается при больших давлениях. На рис. 1.11 показана также измеренная в статических условиях при 888 К часть переходной кривой диссоциации N20, соответствующая области низких давлений [666]; в противоположность диссоциации больших многоатомных молекул сдвиг переходной области реакции в сторону меньших давлений при уменьшении температуры оказывается исключительно слабым. [46]
Вторичные комплексы разлагаются значительно медленнее, и константы скорости первого порядка для гидроперекисей этила и метила имеют значения, равные соответственно 2 3 10 J и 4 10 - 3 сек. [47]
R - газовая постоянная; v0 - константа скорости первого порядка для разложения взрывчатого вещества при окружающей температуре Т0; W - энергия на единицу объема, выделяемая во время реакции; / С - теплопроводность заряда, 8 - критический параметр, равный 3 5, 8 0 и 13 3 для пластин, цилиндров и сфер соответственно. [48]
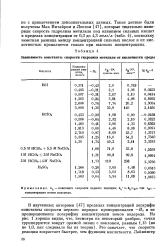 |
Зависимость константы скорости гидролиза метилаля от кислотности среды. [49] |
В изученных авторами [47] пределах концентраций логарифм константы скорости первого порядка пропорционален - Н0 и не пропорционален логарифму концентрации ионов водорода. Это означает, что скорость реакции возрастает быстрее, чем функция кислотности. [50]
Это следует также из того факта, что константа скорости первого порядка не зависит от концентрации. [51]
За исключением особого случая, когда k - константа скорости первого порядка, величина ЕА в формуле (1.6) зависит от того, в каких единицах выражена константа скорости: в единицах концентрации или давления. [52]
Скорость присоединения к крайнему углеродному атому можно охарактеризовать константой скорости первого порядка а относительно концентрации данной растущей на поверхности катализатора углеводородной цепи. [53]
Среднее время жизни протона т непосредственно связано с константой скорости первого порядка. [54]
При взаимодействии пентанола-1 с мочевиной при 147 5 С константа скорости первого порядка k по ходу превращения сильно уменьшается. Это явление отражает тормозящее действие аммиака. [55]
Страницы: 1 2 3 4