Константа - скорость - реакция - первый порядок
Cтраница 3
 |
Взаимодействие пластин из инертного металла и цинка с серной кислотой в случае, когда пластины не соприкасаются ( слева и соприкасаются ( справа. [31] |
Множитель k называют константой скорости реакции первого порядка. [32]
Таким путем были измерены константы скоростей реакций первого порядка для соответствующей реакции в случае Сг. [33]
По данным Рамспергера, константа скорости реакции первого порядка для распада азометана имеет значение 1 00 х 10 - при 287 3 С и 20 8 X X 10 - при 327 4 С. [34]
В табл. 1 приведены константы скорости реакции первого порядка поглощения отдельных компонентов при разных - температурах и концентрациях серной кислоты. Скорость поглощения повышается в ряду пропадиен-метилацетилен-винил-ацетилен. Для каждого компонента скорость поглощения возрастает при повышении концентрации и температуры серной кислоты. Повышение концентраций серной кислоты, по-видимому, более выгодно, чем повышение температуры. Так, при температуре 25 С скорость поглощения пропадиена повышается в 3 5 раза при увеличении концентрации на 5 %, тогда как при повышении температуры с 25 до 45 С скорость поглощения возрастает лишь в 1 8 - 2 7 раза. В условиях наших опытов скорость поглощения ацетилена серной кислотой лежит на пределе чувствительности данной методики. В табл. 2 приведена рассчитанная по уравнению реакции первого порядка константа скорости хемосорбции. [35]
Как видно, величина константы скорости реакции первого порядка не зависит от способа выражения концентраций. [36]
 |
Скорость реакции инверсии тростникового сахара. [37] |
Это соотношение показывает, что константа скорости реакции первого порядка обратно пропорциональна периоду полураспада. [38]
 |
Константы скорости ( k, c - реакций замещения аква-лигандов в комплексах различных металлов при 25 С [ 1561. [39] |
Класс II-комплексы, для которых константы скорости реакций первого порядка изменяются от ЫО5 до ЫО8 с-1. [40]
Это соотношение показывает, что константа скорости реакции первого порядка обратно пропорциональна периоду полураспада. Кинетическому уравнению ( 307) подчиняются не только мономолекулярные реакции, но и разнообразные другие не мономолекулярные. [41]
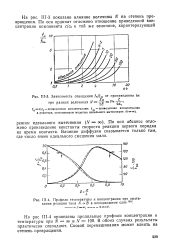 |
Зависимость отношения fn / fx от произведения ki.| Профили температуры и концентрации при протекании реакции типа А - В в неподвижном слое105. [42] |
По оси абсцисс отложено произведение константы скорости реакции первого порядка на время контакта. Влияние диффузии сказывается только там, где число ячеек идеального смешения мало. [43]
В этом уравнении К обозначает константу скорости реакции первого порядка. [44]
Кроме того, найдено, что константа скорости реакции первого порядка, соответствующая исчезновению галогена из водного раствора, при данной температуре прямо пропорциональна площади поверхности металла Q и обратно пропорциональна объему раствора V. [45]
Страницы: 1 2 3 4