Константа - скорость - данная реакция
Cтраница 2
Очевидно, для этого нужно заранее определить константы скоростей данной реакции. [16]
Очевидно, что для такого расчета необходимо заранее определить константы скоростей данной реакции. [17]
Сопоставление двух последних уравнений показывает, что различие между константами скорости данной реакции в газе и в растворе обусловлено различием в величинах термодинамических констант равновесия образования переходного состояния в этих двух фазах и коэффициентов активности. [18]
Кгет: Kjjci, гДе гет и HCl - соответственно константы скорости данной реакции в присутствии гетерогенного ( ОУ, КУ-2, КБ-4П-2) и гомогенного ( HG1) катализаторов, отнесенные к одинаковому числу каталитически активных ионов водорода и выраженные в л / молЬ Сек. [19]
Энергию активации для той или иной реакции можно определить измерением константы скорости данной реакции при двух или нескольких температурах, как описано в примере 10.5. Полученное значение можно затем использовать для расчета скорости реакции при других температурах. [21]
Величины k и fca называются каталитическими константами; они равны константе скорости данной реакции при концентрации катализатора ( НдО 1 или ОН -), равной единице. [22]
Величины k1 и &2 называются каталитическими константами; они равны константе скорости данной реакции при концентрации катализатора ( Н3О или ОН), равной единице. [23]
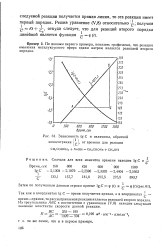 |
Зависимость g С и величины, обратной концентрации ( - i, от времени для реакции. [24] |
Из треугольника ABC в соответствии с уравнением ( V8) находим следующее значение константы скорости данной реакции. [25]
Следовательно, по экспериментальным данным строим график зависимости lg ( a - x) f ( т) и по тангенсу угла наклона, учитывая масштабы координат, определяем константу скорости данной реакции. [26]
Изучение кинетики алкоголиза полиэтиленизофталата этиленгликолем [107] показало, что этот процесс протекает по бимолекулярному механизму. Причем константа скорости данной реакции линейно растет с увеличением концентрации в реакционной среде этиленгликолята, являющегося катализатором процесса. Энергия активации для некатализируемой реакции составляет 32 ккал / моль, а для каталитической 19 ккал / моль. Скорость реакции определяется стадией образования комплекса между эфирной связью и молекулой алкоголята. [28]
Значит, при повышении температуры должна увеличиться и правая часть. Следовательно, константа скорости данной реакции является действительно постоянной величиной только при заданной температуре. Как бы мы ни меняли концентрации веществ А и В, константа скорости от этого не изменится, следовательно она не зависит от концентраций реагирующих веществ. [29]
Отмеченное выше превращение 1 2 3-триметилциклопентанов в 1 1 3-триметилциклопентан в этом смысле особенно характерно. Так, константа скорости данной реакции резко возрастает в ряду: транс транс -; транс цис - и цс, шизомеры. [30]
Страницы: 1 2 3