Константа - скорость - адсорбция
Cтраница 1
Константа скорости адсорбции на металлах обычно высока и сочетается с малой энергией активации; последним членом в уравнении в большинстве случаев можно спокойно пренебречь. Следовательно, этот метод приводит к приближенному значению энергии активации десорбции. [1]
Константа скорости адсорбции на металлах обычно велика, а энергия активации адсорбции мала. [2]
Константа скорости адсорбции / саяс в первом приближении от потенциала не зависит. [3]
Константа скорости адсорбции / из различных солевых растворов остается постоянной, но величина адсорбции оказывается тем выше, чем меньше растворимость иода в данном солевом растворе. Все это находится в полном соответствии с теоретическими представлениями о том, что скорость диффузии растворенных веществ определяется скоростью диффузии молекул растворенного вещества в глубь зерен сорбента. С увеличением объема макропор, являющихся транспортными путями для молекул иода в глубь зерен активированного угля, эта скорость возрастает. Следовательно, процесс адсорбции пода крупнопористыми углями протекает значительно быстрее, чем мелкопористыми. [4]
 |
Кинетические кривые адсорбции при разных температурах. [5] |
Константа скорости адсорбции Ка зависит от температуры и концентрации адсорбируемого компонента. [6]
Зависимость константы скорости адсорбции от потенциала выражается уравнениями, аналогичными уравнениям ( V. В характеризует константу скорости, не зависящую от потенциала. [7]
Отношение констант скоростей адсорбции и десорбции называют адсорбционным коэффициентом Ъ К: К % он характеризует прочность связи веществ с поверхностью. [8]
Зависимость константы скорости адсорбции от потенциала выражается уравнениями, аналогичными уравнениям ( V. В) характеризует константу скорости, не зависящую от потенциала. [9]
Следовательно, константа скорости адсорбции / с уменьшается с увеличением давления. [10]
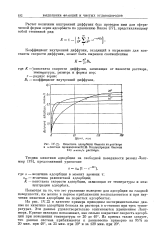 |
Кинетика адсорбции бензола из раствора. [11] |
К - константа скорости адсорбции, зависящая от температуры и концентрации адсорбата. [12]
Ка - константа скорости адсорбции; k - константа скорости реакции на поверхности; F0 - приведенная к 0 скорость газа-носителя; R - газовая постоянная; W к - масса катализатора; - степень превращения. [13]
 |
Синтез аммиака при 450. [14] |
Следовательно, константа скорости адсорбции k уменьшается с увеличением давления. [15]
Страницы: 1 2 3 4