Константа - скорость - гидролиз
Cтраница 4
Аг ] - концентрация остатков аминокислот; [ Р ] - концентрация полипептидов; / q - константа скорости гидролиза внутренних пептидных связей, приводящего к образованию новых полипептидов. [46]
Те же реакции гидролиза поливинилацетата и ацеталирования поливинилового спирта были исследованы Сакурада [14], который получил для констант скорости гидролиза образцов поливинилацетата разной микроструктуры значения, близкие к результатам Фуджи. [47]
При рН 4 и температуре 100 С перхлорат лития уменьшает вдвое, хлористый барий не влияет на константу скорости гидролиза. [48]
Четвертый член уравнения ( 57) К определяет зависимость скорости гидролиза полисахарида от температуры, он находится эмпирически по изменению константы скорости гидролиза. [49]
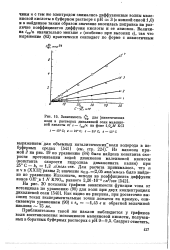 |
Зависимость z j, для [ кинетических волн в растворах дикалиевой соли малеиновои кислоты от с - fnp / x на Фоне 1. Л / KC1. [50] |
Из наклона прямой 2 на рис. 19 по уравнению ( 84) была найдена константа скорости протонизации водой дианионов малеиновои кислоты ( константа скорости гидролиза дималеината калия) при 25 С - АХ 1 2 л / молъ-сек. [51]
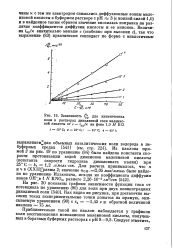 |
Зависимость. / р для кинетических волн в растворах дикалиевой соли малеино-вой кислоты от с - Jnp / x на фоне 1 0 М КС1. [52] |
Из наклона прямой 2 на рис. 19 по уравнению ( 84) была найдена константа скорости протонизации водой дианионов малеиновой кислоты ( константа скорости гидролиза дималеината калия) при 25 С - AI 1 2 л / молъ-сек. [53]
Быстрый переход а-модификации гидроокиси алюминия в бемит в щелочных растворах позволяет с достаточной степенью надежности оценить константы скорости накопления или уменьшения гидроксил-ионов ( эти константы пропорциональны константам скорости гидролиза) только для промежутков времени меньше 60 минут с момента приготовления раствора. Расчет констант скорости накопления и уменьшения ( зона № 3) ионов ОН, проведенный по уравнению реакции 1-го порядка для участков 1 - 2, приводит к значениям констант, соответственно равным ( 5.5 0.7) - 10 - 2, ( 3.0 0.5) - 10 2 и ( 3.6 0.4) - Ю 2 мин. [54]
В согласии с этими величинами для а бикарбоната, определенной обычными аналитическими работах было найдено & Г [ Н2О ] 0 024 - 0 026сек 1, констант скорости гидролиза, полученных аналитическим и, подтверждает гидролитический механизм обмена, осНову расчета. [55]
Рассмотрение полученных данных позволяет установить, что значения констант скорости реакций изученных ФОС изменяются при переходе от вещества к веществу, как правило, симбатно с изменением значений констант скорости гидролиза в слабощелочной среде. Это подтверждает представление офодственности механизмов обеих реакций ( см. схемы на стр. В соответствии с этим изменяются значения и энергии активации, как правило, симбатно для той и другой реакции. Это указывает на решающее значение лабильности одной и той же Р - X -связи в реакции с ХЭ и реакции гидролиза. Вместе с тем необходимо указать, что величина предэкспонента, характеризующая фактор вероятности эффективного соударения молекул, меняется не симбатно в обеих реакциях и тем самым существенно влияет на указанную закономерность. Так, при сопоставлении веществ 2 и 3 видно, что снижение энергии активации не приводит к повышению константы скорости реакции с ХЭ вследствие существенного снижения величины предэкспонента. [56]
Результаты измерения мономолекулярных констант скорости гидролиза и взаимодействия с ацетилхолинэстера-зой ( в сопоставимых условиях) показали, что логарифмы этих величин для исследованной серии соединений приближенно укладываются в линейную зависимость, причем, чем выше константа скорости гидролиза, тем выше и антихолинэстеразная активность. Такой характер зависимости, несомненно, связан с однотипным влиянием электрофильности радикала Аг на обе реакции. Для ароматических радикалов, исследованных Олдриджем и Девисоном, относительная электрофильность может быть количественно оценена величиной константы диссоциации соответствующего фенола Аг - ОН. При этом оказалось, что между силой кислоты Аг-ОН и константами скорости щелочного гидролиза и взаимодействия с холинэстеразами наблюдается определенная зависимость. Аналогичные результаты были получены Кетеларом [149] и другими авторами. [57]
Таким образом, изменение энтропии активации при щелочном гидролизе метоксиметилфторфосфоната оказывается настолько благоприятным по сравнению с изменением энтропии активации щелочного гидролиза изопропоксиметилфторфосфоната, что, несмотря на более высокое значение энергии активации в случае метилового аналога, константа скорости гидролиза метоксиметилфторфосфоната оказалась, как уже отмечалось ранее, почти в 4 раза выше константы скорости щелочного гидролиза изопропоксиметилфторфосфоната. [58]
Страницы: 1 2 3 4