Константа - стабильность
Cтраница 2
На рис. 6.28 показано, какие места занимают двухвалентные ионы металлов на графике зависимости каталитической константы скорости реакции разложения ацетондикарбокси-лата от константы стабильности К. [16]
Потенциометрические измерения в метанольном растворе показали [155], что в случае циклических полиэфиров, содержащих повторяющееся звено - СН2СН2О -, константы стабильности для каждого катиона проходят через максимум при увеличении размера цикла полиэфира. Существует тесная связь между диаметром катиона и диаметром дырки, что следует из измерений оптимального размера цикла полиэфира при образовании комплекса с катионом на моделях. Этому явлению дается объяснение на основании конкуренции между образованием комплекса и сольватацией. [17]
Электроды гетерогенного типа с 8СМ - - функцией получены на основе смеси Ag2S с AgSCN [215]; их применяют для определения констант стабильности роданидных комплексов. [18]
Потенциометрические измерения в метанольном растворе показали [155], что в случае циклических полиэфиров, содержащих повторяющееся звено - CHaCt O -, константы стабильности для каждого катиона проходят через максимум при увеличении раз мера цикла полиэфира. Существует тесная связь между диаметром катиона и диаметром дырки, что следует из измерений оптимального размера цикла полиэфира при образовании комплекса с катионом на моделях. Этому явлению дается объяснение на основании конкуренции между образованием комплекса и сольватацией. [19]
Комплексы между циклическими полиэфирами и ионами с одинаковыми зарядами и не сильно отличающимися диаметрами могут сильно различаться по их относительной стабильности; различие в константах стабильности между Са2 и РЬ2 при образовании комплекса с дициклогексил-18 - краун-6 составляет около 105, комплекс с последним ионом является более прочным. Такое селективное различие может иметь определенную ценность с точки зрения токсичности свинца в некоторых биологических системах. При переходе от полярных к менее полярным растворителям ожидается рост стабильности комплексов. Для комплексов с дицикло-гексил-18 - краун-6 ( 109) константы стабильности в случае ионов К и Na при переходе от воды к метанолу повышаются примерно в 104 и в 103 раз соответственно. [20]
Наблюдаемое заметное различие в хроматографических характеристиках членов одного и того же ряда ( например, 1-фосфата глюкозы, 6-фосфата глюкозы и 1 6-дифосфата глюкозы) объясняется влиянием величин рК фосфатных групп и константами стабильности боратных комплексных соединений. Кроме того, стерические трудности, создаваемые фосфатной группой, могут снизить стабильность комплексного соединения и, следовательно, снизить прочность связывания, фосфата сахара с анионообменной смолой. [21]
Лд-общий коэффициент распределения лиганда А, ЯА - молальный коэффициент распределения свободного незакомплексованного лиганда, МА - концентрация лиганда А в смоле, включая закомплексованные молекулы ( молальная), т - концентрация лиганда А во внешнем растворе ( молальная), Л1М - концентрация металла М в смоле, включая закомплексованные ионы ( молальная), Кг - константа стабильности комплекса с г лигандами. [22]
Жиль-Ав и Херлинг [32] описали определение методом газовой хроматографии констант стабильности комплексов серебро - олефин. Определены константы стабильности шестнадцати комплексов серебро - олефпн [32]; они показывают, что на стабильность комплексов влияют как стерические, так и электронные факторы. Метильные заместители у двойной связи заметно уменьшают стабильность; с увеличением размера заместителя стабильность падает еще больше. [23]
Это говорило о том, что дифенил в твердом состоянии действительно плоский. Так-как константа стабильности его пикрата не отличается от дибензила, следует полагать, что в пикрате он имеет плоскую структуру, что усиливает стабильность комплекса. [24]
Знание констант стабильности позволяет предполагать и быстроту действия соединения. Сведения о сравнительной силе действия солей металлов и их комплексных, в частности хелатных, соединений могут быть использованы при решении вопроса о комплексо-нотерапии отравлений металлами. [25]
Последний комплекс значительно более стабилен. Разница в константах стабильности объясняется не только большей основностью атомов азота в этилендиамине, но и большим энтропийным эффектом в последнем случае. Структура / захватывает ионы К слабее, чем структура Я. [26]
Величины k и ft0 вычисляются из удельных объемов удерживания олефина. Этим методом были подсчитаны константы стабильности шестнадцати комплексов олефинов с серебром. [27]
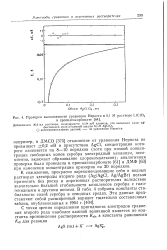 |
Проверка выполнимости уравнения Нериста в 0 1 М растворе LiClO4 в пропиленкарбонате. [28] |
К сожалению, прекрасно зарекомендовавшие себя в водных растворах электроды второго рода ( Ag / AgCl, Ag / AgBr) нельзя применять без риска в апротонных растворителях вследствие значительно большей стабильности комплексов серебра с гало-генидными и другими ионами. В табл. 4 собраны константы стабильности солей серебра в неводных средах. [29]
Тот факт, что прямая на фиг. Так как на абсолютную величину константы стабильности влияют размеры хелатного кольца и ряд других факторов, нельзя ожидать, что прямая с единичным наклоном пройдет через начало координат. Тем не менее прямая на фиг. [30]
Страницы: 1 2 3 4