Константа - тушение
Cтраница 1
Константы тушения как триплетных, так и синглетных возбужденных состояний во всех случаях определяются диффузией или даже превосходят диффузионную константу. [1]
Для статического механизма константа тушения представляет собой константу равновесия образования комплекса в основном состоянии. [2]
Кроме того, они оценили константы тушения флуоресценции бензола диацетилом и кислородом, равные 7 4 - 1010 и 6 4 - 1010 л / молъ-сек соответственно. [3]
Константа К известна под названием константы тушения Штерна - Вольмера. [4]
Примерами подобных реакций могут служить данные по константам тушения триплетных состояний различными водородсодержащими добавками. В этих реакциях тушение триплета проходит с одновременным переносом водорода. Наиболее эффективными тушителями триплета с переносом водорода являются, например, котоспирты и гидрохиноны. Однако применение Итон реакции высоко специфично, и для каждого отдельного случая при образовании тех или иных продуктов распада требуется подбор добавки с учетом высоты триплетпых уровней и активности атомов водорода. [5]
Сенсибилизаторы в жидких растворах не фосфоресцируют 1), и прямое измерение констант тушения и времен жизни их триплетных состояний невозможно. В этих случаях перенос возбуждения также идет по обменно-резонансному механизму, поскольку критическое расстояние для переноса энергии близко к диаметру сечения для столкновений. [6]
Разработанная нами фотохимическая методика была использована для сравнения относительного выхода электронно-возбужденного иода при фотолизе CF3J и C3F7J и определения константы тушения иода молекулярным кислородом. [7]
Предполагают, что тушение специально вводимой добавкой, например диацетилом, контролируется диффузией и что время жизни TO можно рассчитать из константы тушения Штерна - Фольмера, используя диффузионную константу скорости тушения, вычисляемую с учетом интересующих условий. [8]
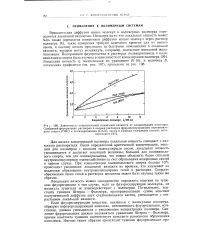
В действительности с помощью фотоэлектрической спектрофотометрической установки были проведены детальные измерения зависимости хода тушения от давления кислорода и для каждого соединения, испытывающего тушение, получены количественные данные о величине константы тушения. В пятой графе приводятся значения длительности возбужденного состояния молекул, полученные из констант тушения паров в предположении, что выход тушащего столкновения равен единице. Справедливость этого предположения была проверена непосредственными измерениями т на флуорометре ФИАНа для спиртового раствора антранола, которые дали для т значение, практически совпадающее с полученным из константы тушения. [9]
Задача 2.10. Определить соотношение между плотностью электронов, ионов и атомов, если ионизация атомов происходит через возбуждение резонансного уровня, который высвечивается за время т, причем резонансное излучение свободно выходит за пределы системы. Константа тушения резонансно-возбужденного состояния & гуш; излучение из других возбужденных состояний не влияет на установление равновесия. [10]
Изучение констант тушения триплетных состояний удобно проводить в вязких растворах. При температурах, близких к комнатной, могут быть использованы растворы 1-бромнафталина в глицерине или полиэтиленгликоле. При низких температурах выбор растворителя более широкий. В качестве тушителя применяют соединения с тяжелыми атомами, кислород, парамагнитные стабильные радикалы, доноры электронов или атомов водорода. Весьма удобным объектом исследования являются соли уранила, флуоресценция которых тушится аминами, спиртами, анионами галогенов и многими другими соединениями. [11]
Локальную вязкость можно одновременно определить опытами по тушению флуоресценции в том случае, если ни флуоресцирующая молекула, ни молекула тушителя не взаимодействуют с полимером. По-видимому, константа тушения Штерна - Фольмера, пропорциональная сумме констант поступательной диффузии двух сталкивающихся частиц, уменьшается с возрастанием локальной вязкости. [13]
Для статического механизма константа тушения представляет собой константу равновесия образования комплекса в основном состоянии. [14]
Следовательно, время жизни молекулы в возбужденном состоянии т, найденное из уравнения ( V-3), составляет величину порядка 10 - 9 сек. Если для другого тушителя константа тушения Штерна - Фольмера меньше, чем для KI, то легко видеть, что не каждое столкновение приведет к тушению. Если константа тушения Штерна - Фольмера берется для флуоресцирующего вещества с тем же временем жизни в возбужденном состоянии и она много больше, чем для К1, то формально этот процесс может быть описан как дальнодействующее взаимодействие ( см. гл. IV, ссылка [12]), эквивалентное большому радиусу столкновения. Однако чаще всего высокие значения констант обусловлены образованием комплексов между тушителем и флуоресцирующей молекулой, неспособных к флуоресценции. Можно ожидать, что спектр поглощения такого комплекса отличается от соответствующего спектра исходной флуоресцирующей молекулы. [15]
Страницы: 1 2