Константа - адсорбция
Cтраница 1
Константа Генри адсорбции быстро уменьшается с повышением температуры. Однако энтальпия адсорбции заметно больше, чем энтальпия испарения, особенно при малых степенях заполнения поверхности, встречающихся в аналитической ГАХ, поэтому зависимость удельных удерживаемых объемов от температуры в ГАХ намного сильнее, чем ГЖХ. [1]
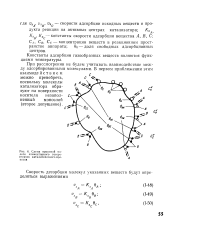 |
Схема принятой модели элементарного гетерогенного каталитического процесса. [2] |
Константы адсорбции газообразных веществ являются функциями температуры. [3]
Влияние констант адсорбции КА и Кв для эндотермических реакций приведено на рис. 7.19 и 7.20 соответственно для последовательного и параллельного отравления. [5]
Чем отличаются константы адсорбции в уравнениях Ленгмюра и Генри и какова взаимосвязь между ними. [6]
Здесь Кр - константа адсорбции ингибитора, А и В - константы, не зависящие от температуры, Qi и Q2 - температурные коэффициенты величин G и Кр соответственно. [7]
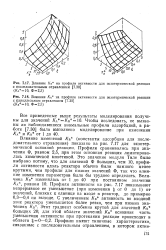 |
Влияние К в на профили активности для экзотермической реакции с последовательным отравлением. [8] |
Влияние изменений / Св ( константы адсорбции для последовательного отравления) показано на рис. 7.17 для экзотермической основной реакции. [9]
Рассмотрим и другие варианты определения констант адсорбции и абсорбции. [10]
Коэффициент / ( называется константой Генри или константой адсорбции. Так как адсорбированные молекулы образуют на поверхности адсорбента монослой, количество адсорбированного вещества пропорционально степени покрытия поверхности или доле монослоя, который образуется. Когда парциальное давление становится более значительным, этот результат осложняют два явления. [11]
Яс - предельная концентрация адсорбированного ПАВ; К - константа адсорбции. [12]
Все эти результаты демонстрируют, что диффузионное сопротивление и константы адсорбции могут серьезно изменить принимаемую картину профилей активности, характеризующих последовательное и параллельное отравление. Это влияние особенно важно для параллельного отравления, при котором нормальный профиль активности может измениться на обратный. Такое аномальное поведение имеет место только для выражения скорости по Ленгмюру - Хиншельвуду, но так как большое число важных реакций, как предполагается, протекает по этому механизму, то должна быть проявлена тщательность в выполнении расчетов профилей активности для таких реакций по всей области модулей Тиле и констант адсорбции. [13]
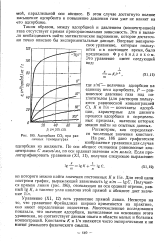 |
Адсорбция СО2 при различных температурах. [14] |
С), К и 1 / п - константы адсорбции, характерные для данного процесса адсорбции в определенных пределах, значение которых можно найти из опытных данных. [15]
Страницы: 1 2 3 4
