Константа - гидролиз
Cтраница 3
Константа гидролиза кислой соли слабой кислоты и сильного основания равна отношению ионного произведения воды к первой константе диссоциации кислоты, соответствующей данной соли. [31]
Константу гидролиза иногда обозначают Kh, однако это совсем не обязательно. Речь идет об обычной константе равновесия основания, непривычным здесь является лишь то, что в качестве основания выступает заряженная частица - ацетатный ион. [32]
Константой гидролиза называется отношение произведения концентраций продуктов гидролиза к концентрации негидролизован-ных ионов соли. Константа гидролиза определяет состояние динамического равновесия, устанавливающегося в растворе данной гидролизующейся соли. [33]
Константой гидролиза называется отношение произведения концентраций продуктов гидролиза к концентрации негидролизован-ных ионов соли. Константа гидролиза определяет состояние динамического равновесия, устанавливающегося в растворе данной гид-ролизующейся соли. [34]
Константой гидролиза / Сг называется отношение произведения концентраций продуктов гидролиза к концентрации негидролизованной соли. [35]
Константой гидролиза Кт называют константу равновесия реакции гидролиза. [36]
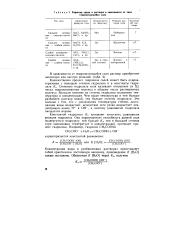 |
Характер среды в растворе в зависимости от типа гидролизующеися соли. [37] |
Константой гидролиза КР называют константу равновесия реакции гидролиза. Она характеризует способность данной соли подвергаться гидролизу: чем больше / СР, тем в большей степени ( при одинаковых температуре и концентрации) протекает процесс гидролиза. [38]
Если константа гидролиза [ см. уравнение ( 16) ] мала, то гидролиз заходит не слишком далеко. [39]
Вычисляются константы гидролиза ( / s) при данной температуре. [40]
 |
Графическое выражение состояния аммиачных растворов. [41] |
Поэтому константа гидролиза имеет примерно одно и то же значение независимо от того, вычисляют ее для аммиачных растворов или нет. Это снова показывает, что в аммиачных раоворах солей бериллия можно полностью пренебречь любой формой образования амминов. [42]
Если константа гидролиза мала и концентрация соли много больше константы гидролиза ( С 10 / СГИдр. [43]
Зная константы гидролиза, вычисляют величины рН гидролизующихся солей по специальным уравнениям. [44]
Если константа гидролиза мала и концентрация соли много больше константы гидролиза ( СКЖгидр. [45]
Страницы: 1 2 3 4