Первая константа - диссоциация
Cтраница 2
Приведена первая константа диссоциации. [16]
Величина первой константы диссоциации определяется, значением т в формуле XOm ( OH) n: если т 0 [ отсутствуют избыточные атомы кислорода по отношению к атомам водорода, как в случае В ( ОН) 31, то кислота очень слабая с А. А Ю 2; при т 2 ( A t: 103) или при то3 ( А Ю8) - кислота сильная. [17]
Величина первой константы диссоциации германиевой кислоты оценивается по-разному. Последняя величина подтверждается также данными кондуктометрического титрования. Такой большой разброс значений можно, вероятно, объяснить различными методами получения двуокиси германия, используемой для приготовления водного раствора. [18]
По первой константе диссоциации двухосновные кислоты являются более сильными кислотами, чем одноосновные. [19]
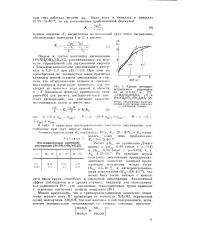 |
Кривые потенцио-мстрического титрования 60 мл - Ю-3 м. [ Pt - ( NH2OH 3NH3 ] C12 ( 1 и [ Pt ( NH2OH 2 ( NH3 2 ] Cl2 ( 2. [20] |
По величине первой константы диссоциации тригидроксил-аминовым комплекс занимает промежуточное положение между тетра - ( А 1а - - - 3.5 - 1 () - 7) и дигидроксиламино-выми комплексами ( А1а 6.0 - 10 8), что может быть также связано с изменением числа групп, способных к кислотной диссоциации. [21]
По величине первой константы диссоциации фосфорной кислоты катионит можно отнести к сильнокислотному, а по величине второй - к слабокислотному типу. [22]
Как видим, первая константа диссоциации значительно больше второй, а вторая больше третьей. При определении концентрации ионов водорода в растворе многоосновной кислоты в большинстве случаев принимают во внимание лишь первую ступень диссоциации, если константа ее не меньше чем в 1000 раз больше константы диссоциации последующей ступени. [23]
Экспериментально полученные значения первых констант диссоциации глицина, а-ала-нина и аспарагина в фазе сульфокатионита близки по величине и значениям первым константам диссоциации этих аминокислот в водных растворах. [24]
В соответствии с первой константой диссоциации сернистой кисло-в водных растворах оксида серы ( IV) при рН 3 0 - 6 0 доминирующей и должны быть бисульфит-ионы. [25]
 |
Зависимость осаждающей способности кислот от их констант диссоциации. [26] |
Для двухосновных, кислот приведена первая константа диссоциации. [27]
В тех случаях, когда первая константа диссоциации очень мала, диссоциация по второй ступени настолько незначительна, что ее нельзя обнаружить. [28]
В тех случаях, когда первая константа диссоциации очень мала, диссоциация по второй ступени настолько незначительна. [29]
В тех случаях, когда первая константа диссоциации очень мала, диссоциация по второй ступени настолько незначительна, что ее нельзя обнаружить. [30]
Страницы: 1 2 3 4