Измеренная константа
Cтраница 1
Измеренная константа передачи цепи в действительности представляет собой усредненное значение констант индивидуальных реакций передачи цепи через различные отдельные атомы ( или, возможно, группы атомов) в молекуле передатчика цепи. Однако благодаря таким факторам, как разница в энергиях связи и стерический эффект, одни атомы участвуют в реакции передачи цепи легче, чем другие. [1]
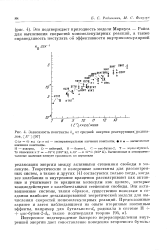 |
Зависимость константы ka от средней энергии реагирующих радика-лов, . [2] |
Теоретические и измеренные константы для рассмотренных систем, а также и других [4] согласуются только тогда, когда все колебания и внутренние вращения рассматривают как активные и учитывают те вращения молекулы как целого, которые взаимодействуют с колебательными степенями свободы. Эти актн-вационные системы, таким образом, существенно помогают в создании наиболее детализированной теоретической модели для вычисления скоростей мономолекулярных реакций. [3]
Теоретические и измеренные константы для рассмотренных систем, а также и других 14 ] согласуются только тогда, когда все колебания и внутренние вращения рассматривают как активные и учитывают те вращения молекулы как целого, которые взаимодействуют с колебательными степенями свободы. Эти актп-вационные системы, таким образом, существенно помогают в создании наиболее детализированной теоретической модели для вычисления скоростей мономолекулярных реакций. [4]
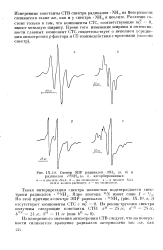 |
Спектр ЭПР радикалов - NH2 ( а, б п радикалов - 15NH2 ( в, г, адсорбированных. [5] |
Измеренные константы СТВ спектра радикалов - NH2 на поверхности силикагеля такие же, как и у спектра - NH2 в цеолите. Различие состоит только в том, что компоненты СТС, соответствующие т - О, имеют меньшую ширину. [6]
Данные, относящиеся к измеренным константам диффузии, где теоретически может ожидаться эффект Тейлора - Голея, взяты в круглые скобки, они не принимались во внимание при усреднении. [7]
Разбавленный водный раствор этилацетоацетата содержит 0 4 % енола ( определенного методом титрования с бромом), а измеренная константа кислотной диссоциации равна 2 - 10-и. Данное значение представляет эффективную константу диссоциации кето-изомера. Поскольку в водном растворе концентрация кето-изомера обычно преобладает над концентрацией енола, последний является обычно более сильной кислотой, хотя это не всегда так. В частности, водный раствор димедона ( 5 5-диметилциклогександион - 1 3) на 95 % состоит из енола и на 5 % из кетона. [8]
Они сравнивали измеренные значения kf с величинами, рассчитанными из данных измерения kb, и константы равновесия реакции; последняя в свою очередь была рассчитана из измеренной константы ионизации нитропарафина и константы диссоциации катализатора - сопряженной кислоты. [9]
В случае принятого выше значения д 0 1 и значения р 0 056, необходимого для согласования g - факторов с экспериментальными данными, уравнения (6.11) можно решить относительно х и Яп ( г - 3У используя измеренные константы сверхтонкой структуры. [10]
Измеренная константа взаимодействия равна 21 5 1 0 гц [28], что находится в хорошем согласии с теоретическим значением. Идентичное значение / гем получено для циклопентен-3 5-диона XXXIV. Как подчеркивают Барфилд и Грант [25], реализацию этих возможностей можно ускорить с помощью более тонких теоретических рассмотрений и уточненных экспериментальных данных. Для иллюстрации необходимости осторожного подхода подчеркнем, что для метиленовых протонов С-4 в XXII / гем18 5 гц [24], хотя рассмотрение модели позволяет предположить, что я-вкладом карбонильной труппы в константу взаимодействия можно пренебречь. Ввиду аналогии, которая существует между циклопропильными и я-системами [29], для объяснения этого разногласия можно привлечь вклад, обусловленный трехчленным кольцом. Аналогично на данном этапе нельзя сказать с уверенностью, является ли увеличение / гем на 2 гц при введении 5-цианогруппы следствием конформационных изменений в кольце А или же оно просто отражает влияние других тонких факторов, таких, например, как слабое изменение угла К-С - Н ( гл. Другие примеры влияния карбонильной группы на константу геминального взаимодействия между протонами соседней метиленовой группы будут приведены в разд. [11]
 |
ЭПР-спектры положительных ион-радикалов. [12] |
ЭПР-спектры таких радикалов дают множество узких линий с хорошо разрешенной сверхтонкой структурой и попадают в категорию ЭПР высокого разрешения. Эти спектры очень удобны для сравнения экспериментально измеренных констант сверхтонкого взаимодействия и рассчитанных по методам валентных связей или молекулярных орбиталей. Такое сравнение требует, однако, очень точного измерения ширин линий и констант сверхтонкого взаимодействия. Такая точность легко достигается с регулятором магнитного поля Филдаля3, который дает истинно линейную развертку. [13]
Этот способ вычислений облегчает также ведение записей в журнале. Следует указать на целесообразность составления карт чистых растворителей - и исследованных ранее смесей, необходимых для ускорения анализов смесей растворителей, В последнем случае в карты полезно заносить, наряду с измеренными константами и прочими сведениями, результаты титрования всех присутствующих функциональных групп, выраженные числом миллилитров нормального раствора на один грамм смеси. [14]
Для очистки кумола от ингибиторов крекинга были применены лучшие из известных методов. Присутствие заметных количеств ингибиторов в кумоле должно оказывать влияние на най - - денное значение константы G. Допустим, что G является измеренной константой, a G - истинной константой. [15]
Страницы: 1 2