Термодинамическая константа - равновесие
Cтраница 3
В полном виде термодинамическая константа равновесия этой реакции выражается соотношением ( ср. [31]
К, - термодинамическая константа равновесия процесса ( для паровой фазы при не слишком больших давлениях K - Kf); С /, С, - концентрации компонентов объемной ( моль / л) и сорбционной ( моль / кг) фаз; у у, - соответствующие коэффициенты активности; р /, р, - стехиометрические коэффициенты сорбции индивидуальных веществ и бинарных смесей. [32]
Исторически точность расчета термодинамических констант равновесия реакции образования сероуглерода соответствовала представлениям о молекулярном составе паров серы при различных температурах и уровню техники эксперимента того времени, когда проводилось исследование. Поэтому данные более поздних работ не согласуются с более ранними, а подчас и противоречат им, особенно в области температур, где молекулы серы диссоциированы до S, не полностью. [33]
 |
Основность типичных представителей важнейших классов органических соединений в водных растворах кислот. [34] |
Величина рКа соответствет термодинамической константе равновесия только в случае слабых оснований, для которых, строго выполняется постулат о коэффициентах активности. Поэтому приводимые здесь значения в большинстве случаев имеют лишь смысл величины Я, необходимой для ионизации основания наполовину. [35]
Для перехода к термодинамическим константам равновесия в эти уравнения вместо концентраций следует подставлять активности. [36]
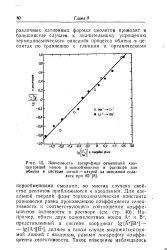 |
Зависимость логарифмов отношений кон. [37] |
Для идеальной твердой фазы термодинамическая константа равновесия равна произведению коэффициента селективности и соответствующего соотношения коэффициентов активности в растворе ( см. стр. Например, обмен двух одновалентных ионов А и В, представленный в системе координат lg [ A ] [ B ] - - lg [ A ] [ B ], должен в таком случае выражаться прямой линией с наклоном, равным логарифму коэффициента селективности. [38]
Отметим также, что термодинамические константы равновесия тоже измеряются в единицах активности. Поэтому измеренные концентрации любых химических форм должны быть переведены в активности перед тем, как их сравнивают с термодинамическими данными. [39]
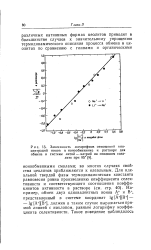 |
Зависимость логарифмов отношений концентраций ионов в ионообменнике и растворе для обмена в системе литий - натрий на основном содалите при 85. [40] |
Для идеальной твердой фазы термодинамическая константа равновесия равна произведению коэффициента селективности и соответствующего соотношения коэффициентов активности в растворе ( см. стр. Например, обмен двух одновалентных ионов А и В, представленный в системе координат Ig [ A ] [ B ] - - Ig [ А ] [ В ], должен в таком случае выражаться прямой линией с наклоном, равным логарифму коэффициента селективности. [41]
Величина Ка носит название термодинамической константы равновесия. Ее численное значение зависит от выбора стандартного состояния. Так как активность - величина отвлеченная, то Ка - безразмерная величина. [42]
Эта величина связана с термодинамической константой равновесия нижеследующим образом. [43]
Константа / Tf называется термодинамической константой равновесия. [44]
С - величина постоянная - термодинамическая константа равновесия, зависящая только от температуры. [45]
Страницы: 1 2 3 4