Последовательная константа - диссоциация
Cтраница 1
Последовательные константы диссоциации этих вещест были определены нами путем потепциометрического титрования. [1]
Рассмотрим расчет последовательных констант диссоциации двухосновной кислоты ( Н2А) по кривой, состоящей из двух буферных областей. [2]
Наблюдаемые соотношения в последовательных константах диссоциации могут быть объяснены с точки зрения взаимного влияния соседних групп. При отщеплении протонов от третьей и четвертой молекул Aldox, помимо уменьшения положительного заряда комплексного иона, играет роль также и присутствие отрицательных групп в цис-положении, приводящее к уменьшению констант. [3]
Большая разница в значениях последовательных констант диссоциации получается по нескольким причинам. Во-первых, чем больше отрицательный заряд основания, тем больше энергия, необходимая для отрыва протона - положительно заряженной частицы. Наряду с общим зарядом сопряженного основания здесь играют роль и взаимодействия между атомами внутри молекулы основания. Относительно небольшой вклад в дифференцирование последовательных констант диссоциации вносит статистический фактор, связанный с вероятностью отрыва одного из двух протонов и присоединения протона к одному или к двум местам в частице основания. Не следует забывать и о том, что у более сильных кислот протоны, образующиеся в первой стадии диссоциации, воздействуют на последующие стадии, смещая равновесие. Поэтому основным источником эффективных ионов водорода является первая ступень диссоциации. [4]
На величину разности между значениями последовательных констант диссоциации влияет взаимодействие групп ОН, связанных с центральным атомом. Если эти группы расположены далеко одна от другой, то такое влияние меньше и, следовательно, отношение последовательных констант также меньше. Последнее значение близко к величине, предусматриваемой для отношения Ха1: Ка2 в случае кислородной кислоты с одним центральным атомом. Отношение Ка2: КаА 1: 10 6 также сравнительно близко к предвиденному значению. [5]
Реакций, при которых отношение последовательных констант диссоциации не соответствует указанному. [6]
Приведенные выше протолитические процессы характеризуются последовательными константами диссоциации. [7]
Это выражение дает величину минимального отношения между последовательными константами диссоциации, при котором еще применим данный метод. [8]
При более детальной характеристике устойчивости комплексных соединений указываются их последовательные константы диссоциации. [9]
Много лет назад Нильс Бьеррум отметил, что отношение последовательных констант диссоциации кислот почти количественно можно объяснить электростатически. [10]
Много лет назад Нильс Бьеррум отметил, что отношение последовательных констант диссоциации кислот почти количественно можно объяснить электростатически. [11]
Описанные методы можно распространить на случай кислот более высокой основности независимо от величины отношения двух последовательных констант диссоциации. [12]
Не придавая этому расчету слишком большого значения, мы все же применили к изучаемым нами соединениям формулу Бьеррума, позволяющую установить связь между отношением последовательных констант диссоциации и расстоянием между отщепляемым протоном и центром тяжести положительных зарядов в молекуле. [13]
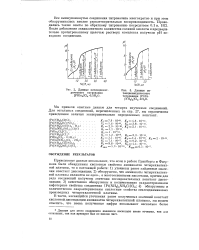 |
Данные потенциомет.| Данные по. [14] |
Приведенные данные показывают, что если в работе Гринберга и Фаер-мана были обнаружены кислотные свойства аммиакатов четырехвалентной платины, то в настоящей работе: 1) уточнены ранее найденные значения констант диссоциации; 2) обнаружено, что аммиакаты четырехвалентной платины являются не одно -, а многоосновными кислотами, причем для ряда соединений получены значения последовательных констант диссоциации; 3) качественно обнаружены и количественно охарактеризованы амфотерные свойства соединения [ Pt ( NH3) 4NH2Cl ] Cl2; 4) обнаружены и количественно охарактеризованы кислотные свойства этилендиаминовых производных четырехвалентной платины. [15]
Страницы: 1 2