Вычисленная константа
Cтраница 1
Вычисленные константы не являются термодинамическими константами рКа поскольку они учитывают концентрации ионной и нейтральной форм вещества, а не их активности. В ряде случаев, когда исследователя интересуют константы основности при сравнении серии соединений, имеющих родственную структуру, можно ограничиться полученными спектрофотометрически константами равновесия. Если необходимо знать термодинамические константы, вносят поправку, которая зависит от ионной силы растворов. Эти поправки, как правило, незначительны, за исключением тех случаев, когда определяются вторые константы ионизации или используются поливалентные буферные соли. [1]
Вычисленные константы близки по значению. [2]
Вычисленные константы k показывают, что реакция имеет первый порядок. [3]
Вычисленные константы диссоциации были сравнены с экспериментальными определениями Штарка и Боденштейна; совпадение, как видим, исключительно хорошее. [4]
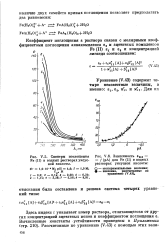 |
Спектры поглощения [ IMAGE ] Зависимость е260. [5] |
Вычисленные константы устойчивости приведены в Приложении ( стр. [6]
Вычисленная константа Кк несколько изменяется с концентрацией. Вполне независимой от концентрации является константа диссоциации, вычисленная с учетом ( хотя и слабых) межионных сил ( через активности, см. стр. [7]
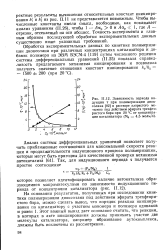 |
Зависимость периода индукции т при полимеризации диоксолана в растворе хлористого метилена под действием эфирата трехфто-ристого бора при 20 С от концентрации катализатора ( М0 4 5 моль / л. [8] |
Чтобы вычисленные константы имели смысл, необходимо, как показывает анализ уравнения (11.26), чтобы 1 - Аар 0 и Аар 1, где А - отрезок, отсекаемый на оси абсцисс. [9]
Соотношение вычисленных констант реакций показывает, что церуссит должен переходить в раствор при значительно меньшей концентрации ионов водорода, чем крокоит. [10]
В табл. 108 приведены вычисленные константы. В некоторых случаях конечные величины были выбраны несколько отличными от округленных величин ввиду их лучшего согласования с другой формулой. [11]
В табл. 108 приведены вычисленные константы. В некоторых случаях конечные величины были выбраны несколько отличными от округленных величин ввиду их лучшего согласования с другой формулой. [12]
Реконструкция спектров на основе вычисленных констант расщепления дала для большинства радикалов ( феназин, р-метил, а - и р-хлор, р-фенил, а-метокси, сс-амино, а-амидные производные феназина) достаточно хорошее согласие с наблюдаемыми спектрами. Найденная на опыте н 1 7 э, по-видимому, является результатом усреднения расщеплений на а - и р-протонах, ввиду ограниченного разрешения прибора. [13]
Впрочем, константа k идентична ранее вычисленной константе k, так как обе они описывают общее потребление кислорода. Вычисленные по формулам значения А и а для стеклян-но-металлического реактора сопоставлены с данными, полученными опытным путем. Как оказалось, последовательно-параллельная схема 2 позволяет удовлетворительно описать кинетику взаимодействия водорода с кислородом в стекляннометаллических реакторах. Таким образом и для данной реакции в довольно широкой области изменения условий процесса установлено постоянство констант в уравнениях, выражающих зависимость выходов от удельной энергии. Это еще раз свидетельствует об удобстве замены времени реакции I удельной энергией. [14]
 |
Зависимость lg A, lg В, lg С и lg D от ЦТ. [15] |
Страницы: 1 2 3 4