Полученная константа
Cтраница 1
Полученная константа и есть константа Михаэлиса. [1]
Полученные константы хорошо согласуются с константами активности, вычисленными для модельных соединений. [2]
Полученные константы не соответствуют литератарным данным для ле-ди-трет. [3]
Полученные константы первого и второго порядка для удобства сравнения с константами однотипных реакций были пересчитаны в константы, выраженные в с 1 и л - моль-1 - с-1 соответственно. [4]
Полученная константа Ка называется термодинамической константой нестойкости. [5]
Полученная константа равновесия тяжелой фракции конденсата находится между гексаном и гептаном. [6]
Все полученные константы имеют один порядок с предсказываемыми теорией, некоторые из них практически не отличаются от рассчитанных по теории Лифшица. Так как все ПАВ, приведенные в табл. 13 ( кроме ксилана - С и сорби-тана - Л), имеют одинаковые олеиновые радикалы, то естественно все различие в константах приписать влиянию полярных групп. Однако оно может быть вызвано не только влиянием полярных групп на ван-дер-ваальсовское взаимодействие, но и различием в электростатическом взаимодействии, которое в этих опытах не исключено и чувствительно к различным поверхностно-активным примесям. [7]
Если полученная константа выгрузки значительно отличается от принятой, проводят повторный расчет распределения и рабочей скорости для нового значения К, которое и будет окончательным, так как изменение К на распределение влияет незначительно. [8]
Постоянство полученных констант нестойкости для различных соотношений компонентов А и В и для изоконцентрат с различной общей моляльностью в свою очередь подтверждает правильность расчетов выходов и равновесных концентраций мономерных молекул А и В. [9]
Постоянство полученных констант нестойкости для различных соотношений компонентов Аи В и для изоконцентрат с различной общей моляль-ностью в свою очередь подтверждает правильность расчетов выходов и равновесных концентраций мономерных молекул Аи В. [10]
Постоянство полученных констант иестойкости для различных соотношении ( компонентов А и В и для изоконцентрат с различной общей молялыгостыо, в свою очередь, подтверждает правильность расчетов выходов и равновесных концентраций мономерных молекул Аи В. [11]
Исходя из полученных констант вычислены скорости окисления ( табл. 3); средняя скорость превращения гексадекана при 160 С в присутствии катализатора ( 0 15 вес. [12]
Для уточнения полученных констант организована процедура случайного поиска [55], заключающаяся в следующем. [13]
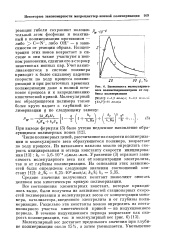 |
Зависимость молекулярного веса полиметакрилонитрила от глубины полимеризации. [14] |
Средние значения полученных констант позволяют описать целиком всю кинетическую кривую полимеризации. [15]
Страницы: 1 2 3 4