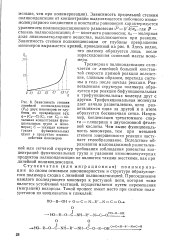
Большая константа - скорость
Cтраница 1
Большие константы скорости для СЮ указывают на заметный - эффект. Так, например, ОН в реакции с катионом иприта [169] примерно в 40 раз более реакционноспособен, чем это следует из уравнения Свэна, которому подчиняются большинство нуклеофилов. [1]
Трехмерная поликонденсация отличается от линейной большей константой скорости прямой реакции. Разветвленная структура полимера образуется при реакции бифункциональных и трифункциональных молекул друг с другом. Трифункциональная молекула дает начало разветвлению, цепи разветвляются одна за другой и в итоге образуется бесконечная сетка. [3]
Прямая или обратная реакция имеет большую константу скорости. [4]
Полученные данные показывают, что более активному катализатору В соответствуют большие константы скорости п и меньшее значение кажущейся энергии активации и температурных коэфициентов скорости реакции. [5]
Полученные данные показывают, что более активному катализатору В соответствуют большие константы скорости ос и меньшие значения кажущейся энергии активации и температурных коэффициентов скорости реакции. [6]
Изомеры исследованных нами непредельных ртутноорганиче-ских соединений, кроме со-меркур-бмс-стильбена, обладают большей константой скорости, чем соответствующие z / wc - соединения. [7]
Сднига метальной и этильной групп в 9 - Х-910 - диметилфена-тренониевых ионах характеризуются значительно большими константами скоростей ( на - 5 порядков), чем в соответствующих 1 - Х-123, 4 5, б-гексаметилбензолониевых ионах. [8]
Метод квазистационарных концентраций ( КСК) [ I ] математически сводится к нахождению асимптотики по большим константам скоростей реакций в уравнениях химической кинетики. Но для многих практических задач представляет интерес распространение квазистационарного приближения и на неизотермические системы. [9]
Схематически изобразить энергетическую диаграмму экзотермической реакции А В ч АВ, Какая реакция - прямая или обратная - характеризуется большей константой скорости. [10]
Как видно из таблицы, винилацетат и метилакрилат имеют приблизительно одну и ту же степень полимеризации, но последний имеет большую константу скорости реакции роста цепи. [11]
Такая аналогия явлений теплопередачи и диффузии была использована рядом исследователей [87, 101], но она справедлива только в предельном случае, при бесконечно большой константе скорости реакции ( диффузионный режим), когда кинетика реакции не играет никакой роли. [12]
Зависимость скорости реакции от температуры можно проиллюстрировать материалами табл. 3.5, в которой приведены данные, касающиеся двух соединений - одного с большой константой скорости, другого - с малой. Если для гексена-1 не удалось определить реального изменения константы скорости, то для малеинового ангидрида наблюдается явное, хотя и небольшое изменение. [13]
В частном случае таким вторым электродом может быть и просто хуже аэрированный или столь же, или даже лучше аэрированный, но имеющий значительно большую константу скорости & а. В последнем случае а-р-элемент образуется не из / - элемента, а из йа-элемента. Kopi, например, определяемый уравнением (1.21) или ( 1 25), независимо от того, каким сочетанием параметров 6ai, & кь kal, k этот потенциал определяется. Исключительно важную роль играет также величина R и соответственно ОПП в среде между электродами. Согласно же экспериментальным и расчетным оценкам для КЭ сталь в глине или сталь в песке превращение а-а-элемента в а-р-элемент требует в большинстве случаев соотношений S2Si, или S2 Si, которые эквива-лентны слабоопасным или неопасным КЭ с крупным анодом и относительно малым, катодом. [14]
В свободном состоянии в газах и жидкостях радикалы достаточно часто при столкновениях оказываются в близком к наиболее выгодному расположению атомов переходном состоянии, что обеспечивает большую константу скорости. [15]
Страницы: 1 2 3 4