Полная константа
Cтраница 2
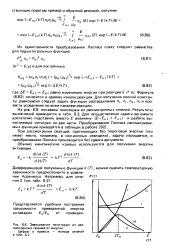 |
Зависимости некоторых из рассмотренных сечений от энергии. [16] |
Формула (8.82) относится к одному каналу реакции. Для получения полной константы равновесия следует задать функции распределения л -, Лу, nkl л / и провести усреднение по всем каналам реакции. [17]
Соли, образованные многоосновными кислотами и многокислотными основаниями, гидролизуются по ступеням. Докажите, что полная константа гидролиза равна произведению констант гидролиза всех ступеней гидролиза. [18]
Соли, образованные многоосновными кислотами и много-кислотными основаниями, гидролизуются по ступеням. Докажите, что полная константа гидролиза равна произведению констант гидролиза всех ступеней гидролиза. [19]
Соли, образованные многоосновными кислотами и многокислотными основаниями, гидролизуются по ступеням. Докажите, что полная константа гидролиза равна произведению констант гидролиза всех ступеней гидролиза. [20]
Легко видеть, что она равна произведению К Кг. В тех случаях, когда константы образования представляют собой полные константы, их обозначают символом р, отличая их таким образом от ступенчатых констант. [21]
Конечно, имеется по одному отдельному слагаемому вида (8.7.37) для каждой пары ядер. Следует отметить, однако, что только возбужденные триплетные состояния дают вклады в полную константу ядерного спин-спинового взаимодействия и что нет никакой естественной нормировки для спиновых плотностей перехода, связывающих состояния различной мультиплетности; те, которые мы использовали, связывают стандартные состояния с MaSa, М 8Ь, и. [22]
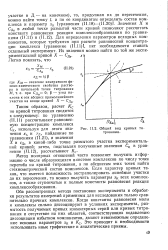 |
Общий вид кривых титрования. [23] |
Метод молярных отношений часто позволяет получить информацию о числе образующихся в системе комплексов по числу точек перегиба на кривой титрования, а по абсциссам этих точек найти стехиометрический состав комплексов. Если характер кривых таков, что имеется возможность экстраполировать линейные участки до их пересечения, то можно получить параметры хк всех комплексов, а также ступенчатые и полные константы равновесия реакции комплексообразования. [24]
Напишите уравнения реакций растворения галогенидов серебра, если в результате реакций образуются стабильные и растворимые в воде комплексные анионы [ Ag ( S2O3) 2 ] 3 - - Напишите схему диссоциации и выражение полной константы образования и константы нестойкости этого комплексного аниона. Значение константы нестойкости комплекса приведено в табл. 8 приложения. [25]
Если точка их пересечения лежит при значении т - Т - 0 5, то это значит, что нейтральных комплексных молекул в растворе не образуется. Если же в точке пересечения т - Т - С 0.5, то в растворе присутствует нейтральный комплекс, доля которого равна 1 - ( т Y -) То - Положение точки пересечения кривых по оси абсцисс просто связано с полной константой нестойкости отрицательно заряженного комплекса. [26]
При более детальной характеристике устойчивости комплексных соединений указываются их последовательные константы диссоциации. Ki Кг дает полную константу нестойкости данного комплекса. [27]
Страницы: 1 2