Диаграмма - равновесие - система
Cтраница 1
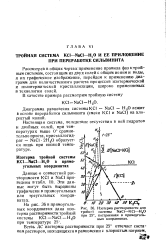 |
Изотерма растворимости для тройной системы NaCl - KC1 - HtO при 25, построенная в прямоугольных координатах. [1] |
Диаграмма равновесия системы КС1 - NaCl - H20 лежит в основе переработки сильвинита ( смеси КС1 и NaCl) на хлористый калий. [2]
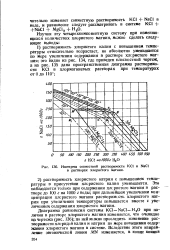 |
Изотермы совместной растворимости КС1 и NaCI в растворах хлористого магния. [3] |
Диаграмма равновесия системы КС1 - NaCl - Н2О при наличии в растворе хлористого магния изменяется, что очевидно 43 чертежа ( рис. 136); по неймсжно проследить изменение растворимости хлоридов калия и натрия по мере повышения содержания хлористого магния в системе. [4]
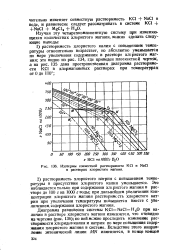 |
Изотермы совместной растворимости КС1 и NaCl в растворах хлористого магния. [5] |
Диаграмма равновесия системы КС1 - NaCl - Н2О при наличии в растворе хлористого магния изменяется, что очевидно 43 чертежа ( рис. 136); по ней можно проследить изменение растворимости хлоридов калия и натрия по мере повышения содержания хлористого магния в системе. [6]
Диаграммы равновесия систем с азеотропизмом в критической области очень сильно отличаются от диаграмм для простых систем. В двойной смеси с положительным азеотропом пространственная критическая кривая имеет температурный минимум. На фазовой диаграмме при этих параметрах появляется двойная критическая точка. При более высоких температурах изотермы равновесия распадаются на две раздельные области, в каждой из которых есть своя критическая точка. [7]
 |
Характеристика процесса ICI. абсорбция S02 раствором основного. [8] |
Диаграмма равновесия системы SO2 - основной сульфат алюминия дана на рис. П1 - 17 а. [9]
Диаграмма равновесия системы кремнезем - окись магния - окись кальция оказывается весьма полезной для исследования сложных реакционных отношений форстерита и монтичеллита в основных магматических породах, в частности, для объяснения образования ме-лилитовых минералов в процессе кристаллизации, важным представителем которых на этой диаграмме служит окерманит. В связи с этой диаграммой Боуэн ш весьма подробно изучил петрогенезис канадских альне-итовых пород. [10]
Диаграмма равновесия системы СО, СОЯ и окислов железа. [11]
 |
Изотерма растворимости для тройнм системы NaCl-KCI - Н О при 25, построенная в прямоугольных координатах. [12] |
Диаграмма равновесия системы KCI - NaCl - H20 лежит в основе переработки сильвинита ( смеси КС1 и NaCl) на хлористый калий. [13]
Диаграмма равновесия системы NaCl - NH4HCO3 - Н2О при других температурах имеет аналогичный характер. Шч, то он увеличивается по направлению к точке Р2, имея, однако, и в точке PI относительно высокое значение. В табл. 38 сопоставлены коэффициенты использования натрия и аммиака в точках PI и Р2 для различных температур. [14]
Страницы: 1 2 3
