Диаграмма - равновесие - система
Cтраница 2
Диаграмма равновесия системы к-гептан - бензол - ди-метилсульфоксид характеризуется закрытой структурой, а при добавлении к диметил-сульфоксиду 12 вес. [16]
 |
Принципиальная технологическая схема установки экстракции диметилсульфоксидом. [17] |
Диаграмма равновесия системы в-г ептан - бензол - ди-метилсульфоксид характеризуется закрытой структурой, а. [18]
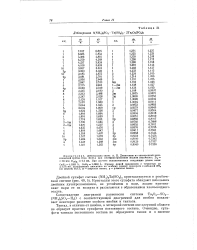 |
Дебаеграмма 6 ( NH4 2S04 - Ta ( S04 5 2Ta202 ( S04 3. [19] |
Сопоставление диаграммы равновесия системы Та205 - S03 - ( NH4) 2S04 - Н20 с соответствующей диаграммой для ниобия показывает некоторое различие свойств ниобия и тантала. [20]
Изучение диаграммы равновесия системы Na2O - PbO - SiO2 дало возможность указать область трудно кристаллизующихся стекол. На диаграмме, эта область очерчена пунктиром. [21]
Часть диаграммы равновесия системы кремнезем - глинозем - окись калия; условия кристаллизации муллита в различных керамических материалах показаны точками на соединительных линиях. [22]
Если известна диаграмма равновесия системы, к которой относится исходное стекло, - сместить его состав к области совместной кристаллизации фаз различного химического состава, пользуясь данными диаграммы равновесия. [23]
На рис. 86 представлена диаграмма равновесия системы МпО - 8Ю2 по Глассеру. [24]
На рис. 107 приведены диаграммы равновесия системы СаО - Р2О5 - N2O5 - Н2О при 100, 50, 25 и 5 С, характеризующие растворимость фосфатов и нитратов кальция в смесях азотной и фосфорной кислот. [25]
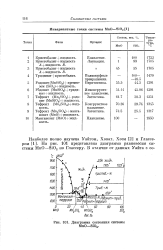 |
Диаграмма состояния системы MnO - Si02. [26] |
На рис. 101 представлена диаграмма равновесия системы MnO - Si02 по Глассеру. [27]
Пфейль, который изучал также диаграмму равновесия системы железо - кислород, показал, что в каждом слое имеется ряд разных соединений. Так, средний слой для образца, окисленного при 1000, состоящий, как ранее предполагали, из магнетита Fe Oa, колеблется по составу железа в пределах 72 35 - 72 5 %; он должен был бы в условиях равновесия содержать 72 35 % железа у наружной поверхности, где он находится в контакте с окис-яой фазой, и 72 5 % у его внутренней поверхности в контакте с закисной фазой. Эта закисная фаза также имеет состав, колеблющийся в широких пределах; в условиях равновесия она содержит лри 1000 75 6 % железа у ее наружной поверхности и 76 9 % у ее внутренней поверхности, но никогда не доходит до 77 75 % - содержания железа, соответствующего формуле FeO, обычно приписываемой закиси железа. Мы поэтому можем, вероятно, найти ее на образцах, нагретых до температуры, выше указанной, и быстро охлажденных. На образцах железа, нагретых в воздухе ниже 575 или даже выше этой температуры и медленно охлажденных, слой закиси железа иожет отсутствовать ( как это было упомянуто в отношении травления на стр. Частичное разложение фазы закисного железа объясняет наблюдение Портевена и его сотрудников, которые установили, что этот самый нижний слой часто разделяется на две части: внутреннюю-гомогенную и внешнюю - с включениями небольших кристаллов магнетита. В течение нескольких часов, как это показали Бенар и Шод - рон2, разложение заканчивается; таким образом на быстро охлажденном железе сохраняется немного закиси железа. [28]
На рис. IX-9, в приведена диаграмма равновесия системы, состоящей из компонентов с ограниченной взаимной растворимостью в твердом состоянии. Здесь линия ликвидуса HEF имеет очертание, аналогичное предыдущему случаю, а линия солидуса HNEMF - более сложное. Область HNPA соответствует твердым растворам а с преобладанием компонента А, а область FMOB - твердым растворам Р с преобладанием компонента В. Область HEN заключает твердый раствор а, изменяющий свой состав с понижением температуры по кривой HN, и жидкую фазу, изменяющую свой состав по линии НЕ. В области РЕМ система состоит из жидкой фазы и твердого раствора р, изменяющих свои составы при понижении температуры соответственно по линиям FE и FM. Область PNEMO заключает смесь твердых растворов аир. [29]
Смесь плавится при температуре около 1800 С с инконгруент-кой кристаллизацией корунда, согласно диаграмме равновесия системы окись алюминия - окись кремния. [30]
Страницы: 1 2 3