Конфигурация - внешний электрон
Cтраница 1
Конфигурация внешних электронов ( 7s) 2 одинакова у всех этих элементов и совпадает с конфигурацией атомов актиния Ас89, - поэтому такие элементы называют актинидами и относят к одной клетке периодической системы элементов, занимаемой элементом актинием. [1]
В свободном состоянии галогены образуют двухатомные молекулы; при этом каждый из атомов приобретает устойчивую октетную конфигурацию внешних электронов. [2]
Анализ многочисленных экспериментальных данных о химических соединениях показал, что химические свойства атомов определяются конфигурацией внешних электронов атома. [3]
Таким образом, возникновение ойъемно-центрированных кубических структур или высокотемпературных модификаций у простых металлов I и II групп и у переходных металлов IV, V и VI периодов, ланта-нидов и актинидов имеет общую причину - - конфигурацию внешних электронов их металлических ионов. В рядах К-Cr, Rb-Mo, Cs - W сильно возрастают температуры плавления, модуль упругости и твердость, характеризующие рост сил межатомной связи Повышение прочности кристаллической решетки внутри групп от Ti, V, Cr соответственно к Hf, Та, W объясняется повышением концентрации электрояисто газа вследствие уменьшения размеров металлических ионов. [4]
Квантовомеханическое толкование связи в этилене сводится к следующему. Сначала конфигурация внешних электронов [ ( 2s) 2 ( 2p) 2 ] свободного атома преобразуется так, что один из ( 2s) - электронов за - нимает ( 2р) - орбиталь. Затем происходит перегруппировка среди двух ( 2р) - электронов и оставшегося одного ( 2s) - электрона, которая ведет к конфигурации, носящей название ( sp2) - гибрида. Для него характерно расположение трех орбиталей в направлении трех вершин треугольника, в плоскости которого лежит центр атома углерода. В отмеченных направлениях орбиталей должны располагаться и химические связи в молекуле. Две орбитали обусловливают связи с атомами водорода, третья преобразуется в ординарную, или а-связь, между углеродными атомами. Ось оставшейся ( 2р) - орбитали перпендикулярна плоскости ( sp2) - гибрида. [5]
Значение 3 85А для расстояния Cs - J - в необнаруженной до сих пор модификации йодистого цезия со структурой хлористого натрия получено путем вычитания 2 7 % из значения, наблюдаемого для кристалла со структурой хлористого цезия; обоснование этого будет дано ниже. Размер иона при этом определяется конфигурацией внешних электронов. Для изоэлектронных ионов это распределение обратно пропорционально эффективному заряду ядра, действующему на электроны. [6]
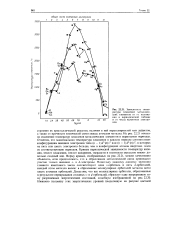 |
Зависимость температуры плавления металлических элементов от i положения в периодической таблице и от числа валентных электронов. [7] |
На рис. 22.21 показано изменение температур плавления металлических элементов в переходных периодах. Отметим, что максимальная температура плавления в каждом периоде соответствует конфигурациям внешних электронов типа ( п - I) d3 ( n) s2 или ( n - ) d ( ri) s2, в которых на пять или шесть электронов больше, чем в конфигурациях атомов инертных газов из соответствующих периодов. Кривые периодической зависимости температур кипения, теплот плазления, теплот испарения, твердости и плотности металлов имеют довольно сходный вид. Форму кривых, изображенных на рис. 22.21, можно качественно объяснить, если предположить, что в образовании металлической связи принимают участие только внешние s - и d - электроны. Поскольку каждому данному значению главного квантового числа соответствуют одна s - орбиталь и пять d - орбиталей, каждый атом металла вносит в образование молекулярных орбиталей металла всего шесть атомных орбиталей. [8]
Sd-орбиталей, которые в поле D5i расщеплены, образуя одноэлектронные а е и ее-орбитали [ 52, стр. При этом, так как ег-орбитали заселены вдвое большим числом электронов [ конфигурация внешних электронов ферроцена есть ( a g) 2 ( eg) ] соответствующий им фотоэлектронный пик имеет в два раза большую интенсивность, чем для aig - состояния. [9]
Наибольшим сродством к электрону характеризуются р-элементы VII группы. Наименьшие ( и даже отрицательные) величины сродства к электрону имеют атомы с конфигурацией внешних электронов ns2 и благородные газы. [10]
 |
Схематические диаграммы расщепления орбит. [11] |
Сравнение электронных конфигураций различных каталитических веществ является весьма перспективным методом исследования. Так, из табл. 3 видно, что все ионы металлов, которые реагируют с водородом в растворе, имеют конфигурацию внешних электронов, соответствующую заполненным или почти заполненным d - оболочкам ( d8 - d10); ионы, обладающие иными электронными конфигурациями, являются неактивными. Чтобы объяснить это, следует проанализировать причины инертности водорода. [12]
В отличие от процессов, приводящих к возникновению рентгеновых спектров, процессы, протекающие на периферии атома, только в незначительной степени зависят от заряда ядра; между атомным номером элемента и его оптическим спектром не существует простой зависимости. Для характера оптического спектра решающим является положение элемента в периодической системе, другими словами, квантовые состояния или, как говорят, конфигурация внешних электронов. Спектры щелочных металлов, например, все принадлежат к одному типу, несмотря на значительную разницу в атомных номерах. [13]
 |
Схема масс-спектрографа. [14] |
Итак, при химических реакциях участие в процессе принимают только внешние электроны; в возникновении характеристических рентгеновых лучей, как уже упоминалось, играют роль, наоборот, внутренние, наиболее близкие к ядру электроны. Но само ядро и в этом случае остается незатронутым; и, пока оно остается неизменным, до тех пор мы вправе говорить о сохранении элемента, ибо все изменения в числе и конфигурации внешних электронов могут быть всегда ликвидированы, и нормальное состояние атома полностью восстановлено; утверждение о неразрушимости химических элементов сводится, таким образом, к утверждению постоянства атомных ядер. Но утверждение это недействительно более в применении к радиоактивным процессам, при которых ядро меняется, теряя свои составные части, в виде а-частиц и - частиц. В результате радиоактивного излучения мы видим образование новых атомов, трансмутацию элементов. [15]
Страницы: 1 2