Конфигурация - благородный газ
Cтраница 3
В табл. 2.9 приведены формулы внешних оболочек электронных конфигураций, перечисленных в табл. 2.8. Нулевая группа характеризуется устойчивыми конфигурациями, так называемыми конфигурациями благородных газов. Далее во втором и третьем периодах последовательно заполняются 2р - и Зр-подуровни. [31]
 |
Расположение координатных осей в тетраэдри-ческом комплексе. [32] |
Теория кристаллического поля объясняет хорошо известный химикам факт, что ионы элементов вставных декад окрашены, в то время как ионы, имеющие конфигурацию благородных газов, бесцветны. В ионах rf - элементов происходит расщепление энергетических уровней валентных электронов в поле лигандов; наоборот, воздействие всех лигандов на s - или р-орбитали одинаково и в этом случае расщепление уровней отсутствует. Становится также понятным, почему ионы Си бесцветны, тогда как ионы Си2 окрашены: ион Си имеет конфигурацию d10; в нем заполнены все d - орбиталн, поэтому переходы электронов с одной cf - орбитали на другую невозможны, у иона Cu2 ( d9) одна d - орбиталь свободна. [33]
 |
Расположение координатных осев в тетраэдря ческой комплексе. [34] |
Теория кристаллического поля объясняет хорошо известный химикам факт, что ионы элементов вставных декад окрашены, в то время как ионы, имеющие конфигурацию благородных газов, бесцветны. В ионах d - элементов происходит расщепление энергетических уровней валентных электронов в поле лигандов; наоборот, воздействие всех - лигандов на s - или р-орбитали одинаково и в этом случае расщепление уровней отсутствует. Становится также понятным, почему ионы Си бесцветны, тогда как ионы Си2 окрашены: ион Си имеет конфигурацию d10; в нем заполнены все d - орбитали, поэтому переходы электронов с одной d - орбитали на другую невозможны, у иона Cu2 ( d9) одна d - орбиталь свободна. [35]
Таким образом, теория кристаллического поля объясняет хорошо известный химикам факт, что ионы элементов вставных декад окр а - - шены, в то время как ионы, имеющие конфигурацию благородных газов, бесцветны. [36]
Из спектров поглощения неорганических атомных ионов известно, что слабо связанные электроны, поглощение которых сильно смещено в длинноволновую область спектра появляются у всех тех ионов, у которых электронные оболочки не имеют законченной конфигурации благородных газов. Сюда относятся в первую очередь ионы переходных элементов, как, например, Fe, Fe, Си, Си, Ru и ионы редких земель. Наоборот, ионы с заполненными оболочками благородного газа, как, например, К, Na, Mg, Ca, F, СГ, поглощают, только начиная с границы кварцевой ультрафиолетовой области; наибольшая прозрачность наблюдается у самих благородных газов. [37]
Ферроцен теряет электрон трудно, поскольку нарушается конфигурация благородного газа. В то же время кобальтоцен легко окисляется до катиона кобальтициния, теряя тридцать седьмой ( разрыхляющий) электрон. Никелоцен с двумя электронами на разрыхляющих орбиталях также может быть окислен, хотя у него удаляется только один электрон с образованием не очень устойчивого катиона никелициния. [38]
Для натрия характерно образование устойчивого иона Na, обладающего электронным строением предшествующего ему благородного газа неона. У иона же хлора строение внешней оболочки соответствует конфигурации благородного газа аргона. [39]
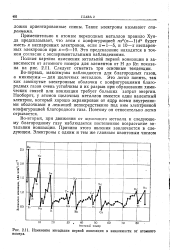 |
Изменение энгадыгаи первой ионизации в зависимости от атомного номера. [40] |
Во-первых, максимумы наблюдаются для благородных газов, а минимумы - для щелочных металлов. Это легко понять, так как замкнутые электронные оболочки с конфигурациями благородных газов очень устойчивы и их разрыв при образовании химических связей или ионизации требует больших затрат энергии. Наоборот, у атомов щелочных металлов имеется один валентный электрон, который хорошо экранирован от ядр всеми внутренними оболочками и лежащей непосредственно под ним электронной конфигурацией благородного газа. [41]
Чем правее расположен неметалл, тем выше энергия ионизации, тем больше сродство к электрону. Поэтому атомы неметаллов проявляют тенденцию к формированию электронной оболочки с конфигурацией благородного газа, что реализуется возрастающей слева направо способностью к присоединению электронов. Внутри групп эти закономерности проявляются снизу вверх, поэтому наиболее электроотрицательным элементом является фтор. [42]
Поляризуемость ионов зависит от типа их электронной структуры, заряда и размера. При одинаковых зарядах и близких радиусах поляризация минимальна у ионов с конфигурацией благородного газа и максимальна у ионов с 18 внешними электронами; а имеет промежуточное значение у ионов переходных элементов с незавершенной - оболочкой. Большая поляризуемость ионов неблагородногазового типа-объясняется большим числом внешних электронов у них. [43]
Поляризуемость ионов зависит от электронной структуры, заряда и размера иона. При одинаковых зарядах и близких радиусах поляризация минимальна у ионов с конфигурацией благородного газа и максимальна - с 18-ти внешними электронами, промежуточное значение а имеют ионы переходных элементов с незавершенной / - оболочкой. Значительная поляризуемость ионов ( / - элементов объясняется большим числом у них внешних электронов. [44]
Поляризуемость ионов зависит от электронной структуры, заряда и размера иона. При одинаковых зарядах и близких радиусах поляризация минимальна у ионов с конфигурацией благородного газа и максимальна - с 18-ти внешними электронами, промежуточное значение а имеют ионы переходных элементов с незавершенной / - оболочкой. Значительная поляризуемость ионов / - элементов объясняется большим числом у них внешних электронов. [45]
Страницы: 1 2 3 4