Конфигурация - инертный газ
Cтраница 3
Галогены имеют большую склонность присоединять один электрон, образуя при этом отрицательные одновалентные ионы с конфигурацией инертного газа ( стр. В этом отношении более энергично реагирует фтор, который, следовательно, является самым электроотрицательным из всех элементов. [31]
Атомы щелочных металлов исключительно легко отдают один электрон, превращаясь в положительные одновалентные ионы с конфигурацией инертного газа. Этим объясняется их очень высокая реакционная способность по отношению к электроотрицательным элементам и многим соединениям, содержащим подобные элементы. [32]
Однако если мы попытаемся разместить электроны вокруг атомов, то увидим, что стремление к достижению конфигурации инертного газа не способствует образованию такого иона. [33]
На этой схеме для элементов 111 и IV периодов конфигурация заполненных внутренних уровней указана с помощью конфигурации инертного газа, у которого заполнены именно эти уровни. [34]
Кроме того, формула ( 2) обычно приводит к катиону, электронная структура которого не достигает конфигурации ближайшего инертного газа. [35]
Простое представление о том, что атом металла принимает столько добавочных электронов, сколько нужно для приобретения конфигурации инертного газа, может быть распространено на карбонил-нитрозилы и гидриды карбонилов. [36]
Атомы этих элементов имеют от одного до трех электронов сверх конфигурации инертных газов и дают катионы с конфигурацией инертных газов. [37]
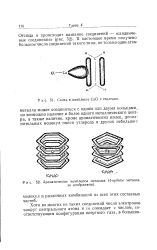 |
Ароматические комплексы металлов ( d - орбиты металла не изображены. [38] |
Хотя во многих из таких соединений число электронов вокруг центрального атома и не совпадает с числом, соответствующим конфигурации инертного газа, в большим. [39]
Изложенный выше способ образования связи между двумя различными элементами является результатом стремления атомов приобрести стабильную конфигурацию, аналогичную конфигурации инертных газов при объединении электронов атомов разных элементов. В приведенном выше примере атом натрия, превращаясь в ион Na, приобретает электронную конфигурацию неона, а атом хлора, став ионом С1 - - электронную конфигурацию аргона. [40]
Ионы элементов главных подгрупп периодической таблицы, например Na, Са2, О2 и С1 -, имеют конфигурацию инертного газа, все их орбитали заняты спаренными электронами и, следовательно, они являются диамагнитными. Ионы многих переходных металлов, а также комплексы этих элементов содержат неполностью занятые электронами орбитали. Для этих элементов ценные сведения получают, используя магнитный метод, как будет показано в соответствующем разделе. [41]
Если способность элементов вступать во взаимодействие сводится к возникновению противоположных зарядов и в конечном итоге к стремлению принять конфигурацию инертного газа, то, конечно, у самих инертных газов нет основания для образования связи. Слишком маловероятно, чтобы они отдали свои крайне прочно связанные электроны другому элементу только для того, чтобы образовать электронную конфигурацию, которая у них уже имеется. Это заключение полностью подтверждается количественным расчетом значений сродства обсуждаемых реакций. [42]
Если способность элементов вступать во взаимодействие сводится к возникновению противоположных зарядов и в конечном итоге к стремлению принять конфигурацию инертного газа, то, конечно, у самих инертных газов нет основания для образования связи. Это заключение полностью подтверждается количественным расчетом значений сродства обсуждаемых реакций. [43]
Если способность элементов вступать во взаимодействие сводится к возникновению противоположных зарядов и в конечном итоге к стремлению принять конфигурацию инертного газа, то, конечно, у самих инертных газов нет основания для образования связи. Слишком маловероятно, чтобы они отдали свои крайне прочно связанные электроны другому элементу только для того, чтобы образовать электронную конфигурацию, которая у них уже имеется. Это заключение полностью подтверждается количественным расчетом значений сродства обсуждаемых реакций. [44]
В результате образуются обычные ковалент-ные связи Мп - Вг длиной 2 53 А, а атомы металла приобретают конфигурацию инертного газа. Интересным здесь является и различие длин связей Мп - С: средняя длина связи атома Мп с атомами углерода карбонильных групп, расположенных в гране-положении к атомам брома, Мп - СОЭКВ. А, заметно короче средней длины ( 1 87 А) других ( аксиальных) связей Мп - СОа1 С. Mn ( CO) sX, объясняется транс-расположением к ним атома брома, отличного по своим свойствам от СО-группы. [45]
Страницы: 1 2 3 4