Электронная конфигурация - атом - инертный газ
Cтраница 1
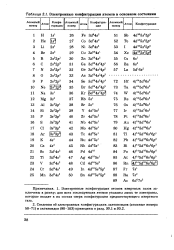 |
Электронные конфигурации атомов в основном состоянии. [1] |
Электронные конфигурации атомов инертных газов заключены в рамку; для всех последующих атомов указаны лишь те электроны, которые входят в их состав сверх конфигурации предшествующего инертного газа. [2]
Аг ] изображена электронная конфигурация атома предшествующего инертного газа. [3]
Ионы этих элементов имеют электронную конфигурацию атомов инертных газов. [4]
Электронная оболочка заполняется целиком, когда достигнута электронная конфигурация атомов инертных газов. [5]
В § 1 было отмечено, что электронная конфигурация атомов инертного газа является наиболее предпочтительной у атомов или ионов, образующих молекулу. Необходимо подчеркнуть, что такая конфигурация является предпочтительной, но не единственной при образовании устойчивых ионов. [7]
Проявляя максимальную валентность 4, атомы титана и его аналогов превращаются в четырехзарядные ионы с электронной конфигурацией атомов инертных газов. Так как во внешнем квантовом слое атомов металлов подгруппы титана только два электрона, то у них отсутствует способность к дополнению внешнего квантового слоя до восьми электронов. [8]
Отдавая три электрона - два с наружного квантового слоя и один с предпоследнего, - атомы элементов подгруппы скандия превращаются в трехзарядные положительные ионы с электронной конфигурацией атомов инертных газов. [9]
Используя уравнение ( 4 - 2) и значения Сп, определенные для галогенидов щелочных металлов, можно найти значение радиусов для всех ионов, имеющих электронную конфигурацию атома инертного газа. Однако определенные таким образом ионные радиусы для всех многозарядных ионов правильно передают только размеры этих ионов относительно ионов щелочных металлов и галогенов. Эти относительные значения называют одновалентными радиусами, они представляют собой те радиусы, которые имели бы многозарядные ионы, если бы они сохранили свое электронное строение и вошли в ионные соединения как однозарядные ионы. К счастью, для многозарядных ионов можно получить имеющие физический смысл кристаллические радиусы гкр из одновалентных радиусов г0, помножив последние на множитель, получаемый из уравнения Борна ( см. стр. [10]
 |
Высшие степени окисления, найденные для некоторых бинарных соединений. [11] |
Для первого ряда внутрирядных переходных элементов ( лантаноидов или 4 / - семейства) соединения со степенью окисления 1П являются не только самыми распространенными для всех членов ряда, но и наиболее устойчивыми, как это видно из табл. 4 - 16; соединения с другими степенями окисления ( 11 и IV) сравнительно редко встречаются. Co степенью окисления IV атом Се приобретает электронную конфигурацию атома инертного газа. Можно предсказать и степень окисления IV у ТЬ, так как в этом состоянии атом тербия приобретает электронную конфигурацию атома Gd со степенью окисления III со сферически симметричным, наполовину заполненным 4 / - подуровнем. [12]
Так, в § 3 мы уже отмечали, что электронная конфигурация атомов инертного газа наиболее предпочтительна для атомов или ионов составляющих молекул, но не единственна. Интересно то, что эта частица состоит из двух протонов и одного электрона. [13]
В основе теории Косселя лежит постулат стабильности электронных конфигураций, свойственных атомам инертных газов: двухэлектрон-ная внешняя оболочка у атомов гелия и восьмиэлектроиная внешняя оболочка в атомах остальных инертных газов. В этом и усматривается причина того, что атомы инертных газов не соединяются ни друг с другом, ни с атомами прочих элементов. Атомы прочих элементов имеют тенденцию принимать электронную конфигурацию атома инертного газа. Это может осуществиться двояким путем: либо посредством захвата электронов извне, либо посредством отдачи всех, электронов внешней незавершенной оболочки. Например, атом серы может включить во внешнюю оболоЧ К у два электрона и принять электронную конфигурацию атома аргона, либо отдать все шесть электронов внешней оболочки - приняв конфигурацию атома неона. [14]
В основе теории Косселя лежит постулат стабильности электронных конфигураций, свойственных атомам инертных газов: двух-электронный внешний слой у атомов гелия и восьмиэлектронный внешний слой в атомах остальных инертных газов. В этом и усматривается причина того, что атомы инертных газов не соединяются ни друг с другом, ни с атомами прочих элементов. Атомы прочих элементов имеют тенденцию принимать электронную конфигурацию атома инертного газа. Это может осуществиться двояким путем: либо посредством захвата электронов извне, либо посредством отдачи всех электронов внешнего незавершенного слоя. [15]
Страницы: 1 2
