Концентрация - донор - протон
Cтраница 1
Концентрация доноров протонов в растворителях с низкой диэлектрической проницаемостью, по-видимому, не существенна для протекания реакции с сохранением конфигурации. [1]
Различие в концентрациях доноров протонов у поверхности электрода и в объеме раствора, как следует из уравнения ( 24) г зависит от величины ifo, поэтому в случае процессов с предшествующей протонизацией ( когда Ei / 2 волн зависят от рН [9,12]) изменение рН в приэлектродной области является дополнительным фактором, влияющим на Е 2 волн при изменении строения двойного слоя. [2]
Наконец, если концентрация доноров протонов очень мала, бианионы могут положить начало ионной полимеризации акрилонитрила ( подробнее см. гл. [3]
При сильном снижении концентрации донора протонов увеличивается время жизни карбаниона и, таким образом, появляется возможность для симметричной сольватации. Явление совершенно аналогично тому, которое обсуждалось в гл. [4]
При р 10 изменение концентрации донора протонов мало влияет на потенциал полуволны. [5]
Экспериментальные данные, полученные при изучении влияния концентрации доноров протонов на предельный ток, зависимость его от рН, опыты по электролизу на стационарном ртутном микроэлектроде вполне согласуются с этими представлениями. [6]
Нетрудно видеть, что соотношение между этими возможными реакциями бианиона определяется концентрацией доноров протона в растворе. [7]
Рядом авторов был прослежен переход одноэлектронного механизма электровосстановления в многоэлектронный при постепенном повышении концентрации доноров протонов в апротон-ной среде или-наоборот, многоэлектронной волны в одноэлектрон-ную при постепенном повышении рН раствора или увеличении доли органической компоненты в водно-органической среде. [8]
На основании концепции Майрановского может быть получено уравнение, аналогичное уравнению ( 89), в котором вместо [ Н ] будет стоять концентрация доноров протонов. [9]
Стадия протонизации, которая независимо от каталитического выделения водорода имеет место во многих электродных процессах восстановления органических соединений, была использована для косвенного определения концентрации доноров протона. [10]
Следует подчеркнуть, что указанные изменения E / z могут наблюдаться [204] только для процессов восстановления с предшествующей поверхностной протонизацией при условии выполнения больцмановского распределения концентрации доноров протонов в приэлектродном слое. [11]
Следует подчеркнуть, что указанные изменения Ei / a могут наблюдаться [204] только для процессов восстановления с предшествующей поверхностной протонизацией при условии выполнения больцмановского распределения концентрации доноров протонов в приэлектродном слое. [12]
Для нахождения истинных констант скорости, не искаженных влиянием двойного слоя, необходимо определяемые непосредственно из опыта кажущиеся значения частных констант протонизации k ( равные наклону прямых зависимости р от концентрации данного донора протонов раствора) экстраполировать к бесконечно большой толщине реакционного слоя, при которой не сказывается влияние поля электрода. Эта зависимость для объемных каталитических волн имеет прямолинейный характер [87], и величина k, экстраполированная к [ H ] - 1 - 0, отвечает истинной константе скорости пере-дачи протона от донора к молекуле катализатора. [13]
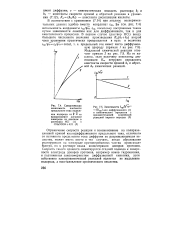 |
Схематическая зависимость плотности предельного тока выделения водорода от V ш на вращающемся дисковом электроде из платины в растворах НС1 ( / и CHsCOOH KCl ( 2.| Зависимости пр. [14] |
Ограничение скорости реакции и возникновение на поляризационной кривой квазидиффузионного предельного тока, отличного-от истинного предельного тока диффузии по разряжающемуся веществу, может иметь место в тех случаях, когда образование реагирующих на электроде протонированных частиц происходит быстро, но в растворе низка концентрация доноров протонов. Скорость такого процесса лимитируется стадией подвода к поверхности электрода доноров протонов, например ионов гидроксония, и подчиняется закономерностям диффузионной кинетики, хотя собственно электрохимической реакцией является не выделение водорода, а восстановление органического вещества. [15]
Страницы: 1 2