Концентрация - анилин
Cтраница 2
После длительного электролиза наблюдается появление устойчивых потенциалов анода, мало изменяющихся сразу после выключения и включения тока и зависящих от концентрации анилина. Данные, касающиеся этих потенциалов, будут рассмотрены в другой работе. [16]
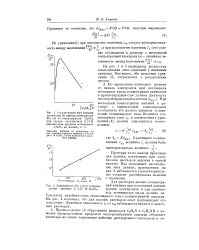 |
Зависимость d In i / dt от концентрации анилина в 0 25 М H2SC4. [17] |
Для растворов разных концентраций анилина при постоянной концентрации электролита и при одинаковых потенциалах анода должна наблюдаться линейная связь стационарного тока с концентрацией анилина. На рис. 4 показано, что для кислых растворов опыт подтверждает это положение. Линейная зависимость гс от сан наблюдается также и в щелочных растворах. [18]
Реакционноспособные сложные эфиры, такие как я-нитрофе-нилацетоацетат [50] могут гидролизоваться по механизму Е сЬ, что определено по отсутствию зависимости скорости реакции от концентрации анилина при образовании ацетоацетанилида в водном буферном растворе. [19]
 |
Кинетические уравнения и скорости реакций. [20] |
На катализаторе АП-56 изучено также окисление анилина в интервале температур 200 - 350 С, объемной скорости потока воздуха 250 - 10000 ч - 1 и концентрации анилина ( 0 5 - 24) х х 10 - 6 ммоль / л [140] и показано, что при 200 - 240 С реакция протекает в кинетической области, а дальнейшее повышение температуры переводит реакцию во внутреннедиффузионный режим. [21]
Другой пример ( прямая / /, рис. 44) относится к системе анилин - толуол - н-гептан ( табл. 3), в которой х представляет концентрацию анилина в анилиновой фазе, а у - концентрацию гептана в гептановой фазе. [22]
Другой пример ( прямая / /, рис. 44) относится к системе анилин - толуол - н-гептан ( табл. 3), в которой х представляет концентрацию анилина в анилиновой фазе, а у - концентрацию гептана в гептановой фазе. [23]
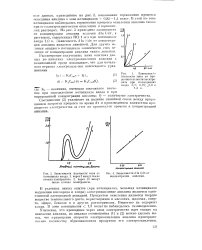 |
Зависимости плотности тока от продолжительности электролиза при потенциалах анода 0 7. 0 75. L0 8 и 1 2 и.| Зависимости плотности тока от.| Зависимости d In i / dt от концентрации анилина. [24] |
Соотношение ( 2) указывает на наличие линейной связи между приращением скорости процесса за время dt и произведением количества прошедшего электричества за этот же промежуток времени н концентрацией анилина. [25]
Результаты собраны в табл. 27, откуда видно, что скорость в отсутствие анилина ( k) и в присутствии последнего ( кт) является линейной функцией отношения концентрации анилина и циклогексена. [26]
Экспериментально обнаружено, что водный раствор анилина в концентрации 300 мг / л через 2 суток приобретает желтоватую окраску ( при высоте жидкости 20 см), а при концентрации анилина 200 мг / л желтоватая окраска появляется на 7 - е сутки от начала опыта. При дальнейших наблюдениях за интенсивностью окраски указанных выше растворов было отмечено усиление интенсивности цвета, что можно объяснить образованием хинонов или их производных, конечным соединением которых является-черный анилин. Анилин в определенных концентрациях прядает воде посторонний привкус. Если же концентрация растворов анилина ниже пороговой по запаху, то привкуса не обнаруживается. [27]
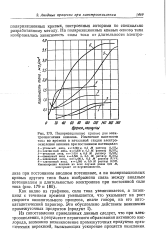 |
Поляризационные кривые для электроокисления анилина. Изменение плотности тока во времени в начальной стадии электроокисления анилина при постоянном потенциале. [28] |
Концентрация анилина во всех случаях равна 0 01 М, электролит не перемешивается. [29]
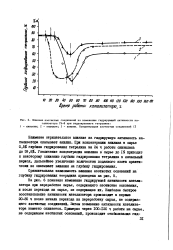 |
Влияние азотистых соединений на изменение гидрирующей активности катализатора ГК-8 при гидрокрекинге тетралина. 1 - хинолин. 2 - пиридин. 3 - анилин. Концентрация азотистых соединений 1 %. [30] |
Страницы: 1 2 3 4