Концентрация - анион
Cтраница 1
Концентрация анионов в массе раствора в случае очень слабой кислоты ( как, например, борная) принимается равной нулю. [1]
Концентрация анионов [ An - ] слагается из концентраций анионов кислоты и анионов соли. [2]
Концентрация аниона ацетил ацетона, достаточная для образования заметных количеств ацетилацетоната металла. [3]
Концентрация аниона, образующегося в результате диссоциации слабой кислоты Н2А по II ступени, численно равна К. [4]
Концентрация аниона в свою очередь является функцией концентрации водородных ионов. [5]
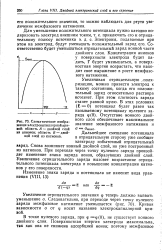 |
Схематическое изображение электрокапиллярной кривой. область А - двойной слой из анионов. область В - двойной слой из катионов. [6] |
Концентрация анионов у поверхности электрода будет падать, Г будет уменьшаться, а поверхностная энергия возрастать, что находит свое выражение в росте межфазового натяжения. [7]
Концентрация анионов СН3СОО - в растворе слагается из концентрации анионов кислоты и соли. Но степень диссоциации уксусной кислоты весьма мала, а в присутствии соли, дающей одноименный анион, она еще более снижается и практически становится весьма незначительной величиной. [8]
Концентрация анионов СН3СОО - в растворе слагается из ко: центрации анионов соли и кислоты. [9]
Концентрация анионов СН3СОО - в растворе слагается из концентрации анионов соли и кислоты. Но степень диссоциации уксусной кислоты незначительна, а в присутствии соли, содержащей одноименный анион, она еще более снижается и практически ее можно не учитывать. [10]
Концентрация анионов может меняться вследствие либо увеличения концентрации соли уранила, либо добавления другого соединения того же аниона, например соли щелочного металла или свободной кислоты. [11]
Концентрация анионов [ А - ] слагается из концентраций анионов кислоты и анионов соли. [12]
Концентрация анионов Н5ОГ принимается равной общей концентрации серной кислоты. [13]
Концентрация аниона А2 - в растворе двухосновной кислоты Н2А, для которой KX Ка, приблизительно равна второй константе диссоциации кислоты. [14]
Концентрация аниона, образующегося в результате диссоциации слабой кислоты Н2А по II ступени, численно равна К. [15]
Страницы: 1 2 3 4