Концентрация - анион
Cтраница 3
Концентрацию аниона А легко рассчитать из общей концентрации органического реагента СНА. Допустив, что общая концентрация металла см пренебрежимо мала по сравнению с концентрацией реагента, СНА можно считать равной сумме концентраций всех форм реагента в обеих фазах. [31]
Концентрацию анионов [ СН3СОО - ] можно принять равной концентрации соли [ CH3COONa ] 0 2 М, так как образование анионов СН3СОО - в результате диссоциации уксусной кислоты происходит в очень малой степени. [32]
Концентрацию аниона [ X3 - J можно определить из общей аналитической концентрации нитрилтриуксусной кислоты Сх и ее третьей константы диссоциации Каз ( см. разд. [33]
Если концентрация анионов в пробе превышает концентрацию выбранного калибровочного раствора, то проводят повторную калибровку и анализ. В начале каждого измерения и после каждой серии анализов следует проверять калибровку по минимум двум калибровочным растворам. [34]
Если концентрация анионов в пробе превышает концентрацию выбранного калибровочного раствора, то проводят повторную калибровку и анализ. В начале каждого измерения и после каждой серии анализов следует проверять калибровку минимум по двум калибровочным растворам. [35]
 |
Константы основности слабых оснований для их водных растворов. [36] |
Поэтому концентрация анионов S2 и РО - незначительна. [37]
Когда концентрация анионов индикатора равна концентрации молекул его рНрК - Значение рН раствора, при котором индикатор ионизирован как раз наполовину, называют точкой перехода индикатора. В этой точке раствор показывает промежуточную окраску. Чем больше отличается рН раствора от рН точки перехода, тем больше отношение концентраций обеих окрашенных форм и тем менее чувствителен индикатор к изменению, рН раствора. Интервал величины рН, в пределах которого изменение окраски можно уловить простым глазом, называют зоной перехода окраски. Область применения данного индикатора для количественного определения рН ограничивается его зоной перехода. [38]
Увеличение концентрации аниона ( катиона) влечет за собой увеличение коэффициента распределения и, кроме того, это вызывает увеличение, что также увеличивает коэффициент распределения. Полимеризация в органической фазе вызывает увеличение коэффициента распределения. Разбавление экстрагента инертным растворителем снижает коэффициент распределения. [39]
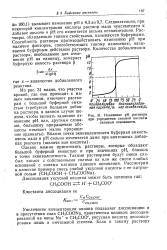 |
Изменение рН раствора. [40] |
Увеличение концентрации аниона подавляет диссоциацию и в присутствии соли CH3COONa, практически целиком диссоциированной на ионы Na и СН3СОО, уксусная кислота диссоциирована лишь в ничтожной степени. [41]
Изменение концентрации аниона в подобном случае влияет на активность катиона лишь вследствие изменения ионной силы раствора. [42]
 |
Изменение рН раствора. [43] |
Увеличение концентрации аниона подавляет диссоциацию и в присутствии соли CHgCOONa, практически целиком диссоциированной на ионы Na - и СН3СОО, уксусная кислота диссоциирована лишь в ничтожной степени. [44]
Изменение концентрации аниона в подобном случае влияет на активность катиона лишь вследствие изменения ионной силы раствора. [45]
Страницы: 1 2 3 4