Концентрация - ион - натрий
Cтраница 2
 |
Роль мицеллы в подавлении флокуляции, вызываемой ионами. [16] |
Действие на концентрацию ионов натрия в растворе менее значительно. [17]
Представления об изменениях концентраций иона натрия ( Na) и хлора ( Cl -) основаны на ископаемых отложениях галита. Общий объем известных отложений галита достигает около 30 % от содержания NaCI в современных океанах. Если всю эту соль добавить в существующие океаны, соленость морской воды увеличилась бы примерно на 30 %, что устанавливает верхний предел. Однако основные отложения галита достаточно хорошо распределяются по геологическому времени, и можно предположить, что никогда не было такого периода, чтобы все эти ионы были растворены в морской воде. [18]
По мере того как концентрация ионов натрия понижалась в результате добавления кремневой кислоты, последняя частично агрегировала за счет окружения частиц кремнезема ионами натрия. Таким образом, при осаждении кремнезема на подобных небольших агрегатах образуется золь с размерами частиц 20 - 250 нм. [19]
Равновесие этой реакции зависит от концентрации ионов натрия и значения рН раствора. [20]
Равновесие наступает, когда градиент концентрации ионов натрия становится равным градиенту концентрации протонов, поддерживаемым внешним источником - дыханием. [21]
Достигаемое при этом резкое увеличение концентрации ионов натрия сдвигает равновесие в сторону недиссоциированных молекул красителя, которые затем, под влиянием внесенного электролита, ассоциируются в более крупные частицы, выделяющиеся в осадок. [22]
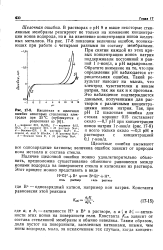 |
Кислотная и щелочная ошибки некоторых стеклянных электродов при 25 С ( публикуется с разрешения из. [23] |
При снятии каждой из этих кривых концентрацию ионов натрия поддерживали постоянной и равной 1 г-ион / л, а рН варьировали. Обратите внимание на то, что при определении рН наблюдается отрицательная ошибка. Такой результат наводит на мысль, что электрод чувствителен к ионам натрия, так же как и к протонам. Это наблюдение подтверждается данными, полученными для растворов с различными концентрациями ионов натрия. [24]
В качестве критерия полноты обмена была выбрана концентрация иона натрия в фазе ионита к концу реакция. [25]
Необходимо отметить, что при под-щелачиваиии возрастает концентрация ионов натрия, а следовательно, увеличивается молярность раствора А. При элюйровании раствором В маркером служит гистидин. Если рН раствора слишком высокий, пик гистидйна накладывается на пик аммиака, а если слишком низкий - увеличивается время, необходимое для элюирования. [26]
Расширение диапазона измерения концентрация натрия позволит оперативно контролировать концентрации ионов натрия в процессе подготовки ее в цехах химоС: ссоливания тепловых и атомних электростанций на всех ступенях ее очистки. Известно [23], что концентрация атрия является осьовккм параметром, характвризувщим качество воды, а такие оптимальный режи:; работы катионитовых фильтров в цехях водоподготовки. [27]
 |
Кривые комплексонометрического титрования. [28] |
Излом кондуктометрической кривой в точке эквивалентности объясняется ростом концентрации ионов натрия за счет диссоциации избытка натриевой соли ЭДТА. [29]
При болезни Аддисона расстройства обмена выражаются резким снижением концентрации ионов натрия и хлора и повышением уровня ионов калия в крови и мышцах, потерей воды организмом и снижением уровня глюкозы в крови. Нарушения белкового обмена проявляются снижением синтеза белков из аминокислот и увеличением уровня остаточного азота в крови. [30]
Страницы: 1 2 3 4