Концентрация - ион - натрий
Cтраница 3
С ростом плотности тока и с повышением криолитового отношения электролита увеличивается концентрация ионов натрия у катода и соответственно повышается активность натрия, растворенного в алюминии и электролите. [31]
С ростом плотности тока и с повышением крнолитового отношения электролита увеличивается концентрация ионов натрия у катода и соответственно повышается активность натрия, растворенного в алюминии и электролите. [32]
Несмотря на то, что концентрация стрептомицина в 300 раз меньше концентрации ионов натрия, последние оказывают весьма малое влияние на сорбцию стрептомицина в случае значительного разбавления раствора. [33]
Можно утверждать, что в определенных условиях - рН 7, концентрация ионов натрия 0 2 М и температура 25 - нативная ДНК имеет характерную и весьма стабильную конформацию. [34]
С ростом илотности тока и с повышением криолитового отношения электролита увеличивается концентрация ионов натрия у катода и соответственно повышается активность натрия, растворенного в алюминии и электролите. [35]
При неизменных температуре колонки, концентрации цитрат-ионов и скорости течения буфера уменьшение концентрации ионов натрия приводит к задержке выхода большинства аминокислот. При уменьшении нормальности третьего буфера с 1 8 до 1 4 не только задерживается элюирование основных аминокислот, но и значительно понижается фоновая линия, обычно наблюдаемая при большей концентрации буфера. [36]
Одноколоночный метод анализа, смола UR-40, Поддерживая постоянными температуру колонки, концентрацию ионов натрия и цитрат-ионов и скорость течения буфера, варьируют величину рН первого буфера. Понижение рН с 3 545 до 3 515 ухудшает разделение треонина и серина ( отношение высоты впадины к высоте пика равно 0 07; определение этого понятия см. в разд. Увеличение рН второго буфера с 4 25 до 4 30 при прочих неизменных условиях анализа ухудшает разделение изолейцина и лейцина. При увеличении рН третьего буфера гистидин элюируется быстрее. [37]
На рис. 1 ( а и б) показана зависимость сорбции стрептомицина от концентрации ионов натрия в растворе ( cNa) для ряда карбоксильных катионитов. Как видно из приведенных результатов, после прекращения обмена во всех случаях количество стрептомицина, сорбированного катионитом, падает по мере возрастания cNa в растворе. [38]
Френкель и Хейнц [10] исследовали только кислые растворы, причем в процессе опыта концентрация ионов натрия в растворе менялась очень слабо. [39]
Так же, как и при анализе кислых и нейтральных аминокислот, уменьшение концентрации ионов натрия приводит, как правило, к задержке элюиро-вания аминокислот. [40]
Поддерживая постоянными концентрацию цитрат-ионов, температуру колонки и скорость течения буфера, варьируют концентрацию ионов натрия в третьем буфере. При уменьшении нормальности буфера с 1 4 до 1 0 триптофан элюируется быстрее, а аргинин медленнее. Кроме того, при меньшей нормальности третьего буфера фоновая линия становится ниже. В общем уменьшение концентрации ионов натрия задерживает выход большинства аминокислот. [41]
Оцененная на основании молекулярных размеров ДСН и степени агрегации, равной 62 [21], концентрация ионов натрия в слое Штерна. [42]
В биологических системах внутри клетки концентрация ионов калия обычно высока, а вне ее высока концентрация ионов натрия. По обе стороны от клеточной мембраны, разделяющей внешнюю и внутреннюю области, присутствует некоторое количество анионов, главными из которых являются ионы хлора. Именно эти три иона ( К, Na и СГ) управляют электрической активностью большинства живых клеток. Поскольку общие концентрации растворов - внешнего и внутреннего - равны, уравнение ( II 1.96) для трех основных ионов, создающих электрический потенциал мембраны, остается в силе. [43]
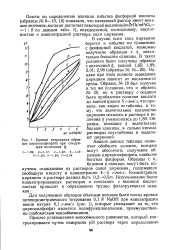 |
Кривые титрования образцов цирконилфосфата при следующих величинах &. [44] |
Для полученных образцов обычным методом были сняты кривые потенциометрического титрования 0 1 N NaOH при концентрации ионов натрия 0 1 г-экв / л ( рис. 1), которые указывают на то, что цирконилфосфат является полифункциональным, преимущественно слабокислым ионообменником. [45]
Страницы: 1 2 3 4