Концентрация - ион - хлор
Cтраница 4
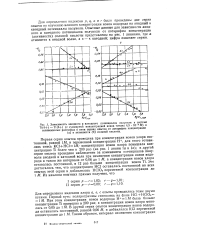 |
Зависимость анодного и катодного потенциалов полуволн в системе. [46] |
Первая серия опытов проведена при концентрации ионов хлора постоянной, равной Ш, и переменной концентрации Н, для этого готовилась смесь КС1Н - НС1 Ш; концентрация ионов хлора повышала концентрацию Ti более чем в 200 раз ( на рис. 1 линии la и 1к); в другой серии опытов проведено наблюдение за изменением потенциалов полуволн анодной и катодной волн при изменении концентрации ионов водорода в таком же интервале от 0 06 до 1 М, а концентрация ионов хлора оставалась постоянной, в 12 раз больше концентрации ионов Ti. [47]
 |
Нормальный каломельный электрод. [48] |
Потенциал такого электрода зависит от концентрации ионов хлора и, следовательно, от концентрации хлористого калия. При постоянной концентрации последнего потенциал обнаруживает хорошее постоянство при каждой данной температуре. [49]
 |
Зависимость растворимости AgCl от концентрации ионов хлора по данным Форбеса ( lg Ag как функция IgCjvici где M NH4, Na и Н. [50] |
При этом принято, что концентрация ионов хлора приблизительно пропорциональна общей концентрации хлорида. [51]
В морской воде, где концентрация ионов хлора велика, скорость коррозии с увеличением скорости движения будет непрерывно увеличиваться вплоть до величины 6 - 7 м / с, поскольку даже увеличение доставки кислорода к металлу в этих условиях не может привести к пассивности металла. [52]
В морской воде, где концентрация ионов хлора велика, скорость коррозии непрерывно возрастает при увеличении скорости вращения до 6 - 7 м / с, поскольку даже улучшение доступа кислорода к металлу в этих условиях не может привести к пассивации металла. [53]
 |
Зависимость inp от концентрации ионов. [54] |
Однако во всей исследованной области концентраций ионов хлора в растворе этого не происходит. [55]
Соляную кислоту вводят для увеличения концентрации иона хлора, способствующего осаждению сульфата бария. [56]
Скорость реакции обратно пропорциональна квадрату концентрации ионов хлора, поэтому уменьшение концентрации ионов хлора приводит к увеличению скорости реакции. [57]
Для непрерывного измерения и регистрации концентрации ионов хлора ( диапазон 10 - 30 г / л, t 22 - 42 С) в электролите никелирования разработан фоторионометр типа ФМ-VI. Для этой же цели предложен нейтронный абсорбциометр типа АБСОМ. [58]
Уменьшение окислительного потенциала с ростом концентрации ионов хлора отражает процесс координации последних трехвалентным железом. По мере увеличения рН зависимость Е / ( lg [ A ]) ] становится менее выраженной. [59]
Значение рН декомплексообразовання г зависимости от концентрации ионов хлора. [60]
Страницы: 1 2 3 4