Концентрация - осаждаемый ион
Cтраница 1
Концентрация осаждаемого иона играет относительно небольшую роль в осаждении сульфидов, так как малорастворимые сульфиды выпадают из сильноразбавленных растворов, а хорошо растворимые не выпадают даже из концентрированных растворов. [1]
Концентрация осаждаемого иона играет относительно небольшую роль в осаждении сульфидов, так как мало растворимые сульфиды выпадают из сильно разбавленных растворов, а хорошо растворимые не выпадают даже из концентрированных растворов солей. Полнота осаждения в значительной мере зависит от степени насыщения сероводородом раствора, в котором осаждаются сульфиды. [2]
Концентрация осаждаемого иона играет относительно небольшую роль в осаждении сульфидов, так как малорастворимые сульфиды выпадают из сильноразбавленных растворов, а хорошо растворимые не выпадают даже из концентрированных растворов. [3]
Концентрация осаждаемого иона играет относительно небольшую роль в осаждении сульфидов, так как плохо растворимые сульфиды выпадают из сильно разбавленных растворов, а хорошо растворимые не выпадают даже из концентрированных растворов солей. Полнота осаждения в значительной мере зависит от степени насыщения сероводородом раствора, в котором осаждаются сульфиды. [4]
Убывание концентрации осаждаемого иона ( количества осаждаемого иона в 1 л раствора) вследствие увеличения концентрации иона-осадителя представлено гиперболической ветвью 1 на фиг. Кривая 2 соответствует общему содержанию осаждаемого иона в растворе. Точки этой кривой могут быть построены следующим образом. [5]
Очевидной является роль концентрации осаждаемого иона: чем больше [ Ме2 ], тем легче будет достигнуто условие выпадения осадка. [6]
Очевидной является роль концентрации осаждаемого иона: чем больше [ Ме ], тем легче будет достигнуто условие выпадения осадка. [7]
Величина кристаллов зависит от концентрации осаждаемого иона в растворе: чем меньше концентрация осаждаемого иона, тем меньше размеры выпадающих кристаллов. [8]
При повышении концентрации иона-осадителя снижается концентрация осаждаемого иона. Но что происходит при этом с растворимостью. По концентрации какого иона нужно ее рассчитывать: осаждаемого иона или иона-осадителя. Очевидно, растворимость нужно считать по концентрации осаждаемого иона. Но отсюда следует, что по мере увеличения концентрации иона-осадителя растворимость малорастворимого электролита уменьшается. Поскольку растворимость AgCl в чистой воде равна 10 - 5 г-мол / л, следовательно, в данном случае она уменьшилась в 1000 раз. [9]
Из выражения для ПР видно, что концентрация осаждаемого иона сделается равной нулю только в том случае, если концентрация иона-осадителя бесконечно велика. Однако бесконечно большую концентрацию иона-осадителя создать невозможно. Поэтому, как бы ни было мало ПР осаждаемого малорастворимого вещества, никогда нельзя полностью удалить из раствора подлежащий удалению ион осаждением. [10]
Скорость появления осадка при качественных пробирочных реакциях прямо пропорциональна концентрации осаждаемого иона. Иначе обстоит вопрос для реакций, выполняемых на предметном стекле с маленькими каплями. [11]
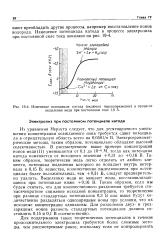 |
Изменение потенциала катода ( включая перенапряжение в процессе выделения меди при постоянном токе 1 0 А. [12] |
Из уравнения Нернста следует, что для десятикратного уменьшения концентрации осаждаемого иона требуется сдвиг потенциала в отрицательную область всего на 0 0591 / л В. Электрогравиметрические методы, таким образом, потенциально обладают высокой селективностью. В рассмотренном выше примере концентрация ионов меди ( II) уменьшается от ОД до I0 - e M, тогда как потенциал катода изменяется от исходного значения 0 31 до 0 16 В. Таким образом, теоретически медь легко отделить от любого элемента, потенциал выделения которого не попадает внутрь интервала в 0 15 В; вещества, количественно выделяющиеся при потенциалах более положительных, чем 0 31 В, следует предварительно удалить. Выделению меди не мешают ионы, восстанавливающиеся при потенциале ниже 0 16 В. Таким образом, если мы будем считать, что для количественного разделения требуется сто-тысячекратное снижение исходной концентрации, то теоретически при разнице стандартных потенциалов 0 3 В или выше будут количественно разделяться однозарядные ионы при условии, что их исходные концентрации одинаковы. Для разделения двух - и грех-зарядных ионов разность стандартных потенциалов должна составлять 0 15 и 0 1 В соответственно. [13]
Быстрота появления осадка, при качественных пробирочных реакциях прямо пропорциональна концентрации осаждаемого иона. Для пробирочных же реакций быстрота испарения растворителя практически равна нулю. [14]
Правило произведения растворимости позволяет также рассчитать концентрацию иона-осадителя, при которой концентрация осаждаемого иона составит заданное численное значение. [15]
Страницы: 1 2 3