Концентрация - восстанавливающийся ион
Cтраница 4
Из рис. 271 видно, что на горизонтальных участках дифференциальной полярографической кривой величина произ - водной равна нулю-приращение силы тока отсутствует; полярографическая волна представляется на дифференциальной кривой в виде пика. Положение пика и его высота характеризуют природу и концентрацию восстанавливающегося иона. [46]
Значение потенциала в данной точке волны так называемого потенциала полуволны будет величиной, которая характеризует природу электровосстанавливающегося или окисляющегося иона в данном фоне. Он, как видно из уравнения, не зависит от концентрации восстанавливающегося иона, но зависит от его природы, так как в уравнение потенциала полуволны входит величина so - нормальный потенциал данного иона. [47]
Потенциал ртутного катода в тот момент, когда достигнута величина напряжения разложения и начинается электролиз, называется потенциалом выделения ( или восстановления) данного иона. Потенциал выделения зависит от природы иона, однако на эту величину оказывает влияние концентрация восстанавливающегося иона и некоторые другие факторы. Поэтому для качественного определения ионов пользуются так называемым потенциалом полуволны, который не зависит от концентрации восстанавливающегося иона. [48]
Потенциал ртутного катода в тот момент, когда достигнута величина напряжения разложения и начинается электролиз, называется потенциалом выделения ( или восстановления) данного иона. Потенциал выделения зависит от природы иона, однако на эту величину оказывает влияние концентрация восстанавливающегося иона и некоторые другие факторы. Потенциал полуволны не зависит от концентрации восстанавливающегося иона. [49]
График строят по данным полярографирования, как правило, не менее чем трех стандартных растворов. На оси ординат откладывается пропорциональная силе диффузионного тока высота полярографической волны, а по оси абсцисс - концентрация восстанавливающегося иона. В соответствии с уравнением (IX.4) калибровочный график должен представлять прямую линию, проходящую через начало координат, и при исследовании многих систем такой график получается в действительности. При отклонении от линейной зависимости приходится увеличивать число стандартных растворов с тем, чтобы увеличить число точек для построения калибровочного графика. Метод дает точные результаты при условии строгой идентичности условий полярографирования стандартных растворов и неизвестной пробы. [50]
Следовательно, при данной концентрации посторонней соли ( и при данной температуре) потенциал полуволны является величиной практически постоянной, не зависящей от концентрации восстанавливающихся ионов. Это свойство Е / 2 чрезвычайно важно для качественного полярографического анализа. Точно так же на потенциал полуволны иона металла не влияет начавшийся ранее процесс восстановления других веществ, а также характеристики капилляра. [51]
Однако к катоду за счет диффузии непрерывно доставляются новые количества ионов, поэтому сила тока не уменьшается, хотя ее рост с увеличением напряжения прекратится. Интенсивность диффузии зависит от разности концентраций у поверхности электрода и во всем объеме раствора. Концентрация восстанавливающегося иона в глубине раствора постоянна; так как электролиз идет при очень небольшой силе тока порядка 10 - 5 А, а концентрация в прикатодном слое близка к нулю. Разность концентраций также постоянна, что и приводит к постоянной скорости поступления ионов к катоду. [52]
Предельный ток зависит от скорости диффузии, а поэтому называется диффузионным. Скорость диффузии достигает некоторого постоянного значения, которое пропорционально концентрации раствора. Поэтому диффузионный ток пропорционален концентрации восстанавливающихся ионов в массе раствора. Следовательно, измеряя диффузионный ток, можно определить концентрацию вещества в растворе. [53]
Потенциал ртутного катода в тот момент, когда достигнута величина напряжения разложения и начинается электролиз, называется потенциалом выделения ( или восстановления) данного иона. Потенциал выделения зависит от природы иона, однако на эту величину оказывает влияние концентрация восстанавливающегося иона и некоторые другие факторы. Потенциал полуволны не зависит от концентрации восстанавливающегося иона. [54]
Острый максимум появляется [56] на площадке волны восстановления ионов кобальта при введении в раствор 8-оксихинолина, не восстанавливающегося в этих условиях. Эти максимумы получили название максимумов 3-го рода [58]; они ПО являются лишь в растворах, тщательно очищенных от посторонних ПАВ. Высота максимумов 3-го рода растет пропорционально концентрации восстанавливающихся ионов. [55]
Острый максимум появляется [56] на площадке волны восстановления ионов кобальта при введении в раствор 8-оксихинолина, не восстанавливающегося в этих условиях. Эти максимумы получили название максимумов 3-го рода [58]; они по-являются лишь в растворах, тщательно очищенных от посторонних ПАВ. Высота максимумов 3-го рода растет пропорционально концентрации восстанавливающихся ионов. [56]
Потенциал ртутного катода в тот момент, когда достигнута величина напряжения разложения и начинается электролиз, называется потенциалом выделения ( или восстановления) данного иона. Потенциал выделения зависит от природы иона, однако на эту величину оказывает влияние концентрация восстанавливающегося иона и некоторые другие факторы. Поэтому для качественного определения ионов пользуются так называемым потенциалом полуволны, который не зависит от концентрации восстанавливающегося иона. [57]
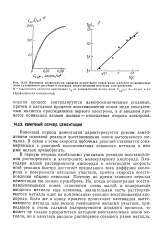 |
Проверка уравнения на примере цементации ионов меди железом из подкисленного сульфатного раствора в условиях перемешивания раствора ультразвуком. [58] |
В первую очередь необходимо учитывать реакцию восстановления растворенного в электролите молекулярного кислорода. Благодаря малой растворимости кислорода в электролите скорость этой реакции быстро достигает предельного тока диффузии кислорода к поверхности катодных участков, причем скорость восстановления обычно невелика. Но, когда концентрация восстанавливающихся ионов становится очень малой, а поляризация анодного металла еще невелика, значительная часть растворяющегося металла идет на компенсацию реакции восстановления кислорода. Если же к концу процесса происходит пассивация вытесняющего металла или резкое уменьшение анодных участков, приводящее к очень сильной поляризуемости анодного процесса, то может не только прекратиться катодное восстановление ионов металла, но и начаться анодное растворение осевшего ранее металла. [59]
Страницы: 1 2 3 4