Концентрация - обменивающийся ион
Cтраница 1
Концентрация обменивающихся ионов в растворе выражается обычно в единицах молярности или моляльности. [1]
С - концентрации обменивающихся ионов i и j соответственно в ионите и растворе, г-экв / кг и г-экв / м3; ki, - коэффициент равновесия ионного обмена, ( кг / м3) 1 / 2 -, ( м / Kr) 1 / zi; Zi и Zj - валентности обменивающихся ионов. [2]
При этом предполагается, что концентрации обменивающихся ионов на границе зерно-пленка ( СА и Св) являются равновесными для данной степени обмена. [3]
Обычно концентрацию каждой фазы выражают через концентрации обменивающегося иона и как части от общей нормальности фазы. [4]
Для разбавленных растворов вместо активностей можно взять концентрации обменивающихся ионов в растворе, так как коэффициенты активности равны единице. [5]
Сорбционное поведение ионов зависит от природы и концентрации обменивающихся ионов ионита, раствора и растворителя. [6]
Равновесие между ионитом и раствором подчиняется закону действующих масс. Повышение концентрации обменивающихся ионов в растворе способствует увеличению степени обмена. При наличии в растворе различных ионов, способных вступать в реакцию обмена, интенсивность обмена будет больше у тех ионов, которые обладают большей прочностью химической связи с активными группами ионита. Повышение относительной концентрации каких-либо из конкурирующих ионов в растворе также способствует увеличению степени их обмена. Изменяя концентрацию ионов в растворе, можно управлять процессом обмена. Так, если катионит находится в Са2 - форме, его можно перевести в Н - форму, промывая катионит в колонке раствором соляной кислоты, хотя химическая связь ионов Са2 с катионитом значительно прочней связи последнего с ионами водорода. При подаче в колонку соляной кислоты в верхней части колонки катионит в Са2 - форме придет в соприкосновение с раствором, в котором концентрация ионов Н постоянно несоизмеримо превышает концентрацию - ионов Са2, и вследствие закона действующих масс будет происходить вытеснение ионов кальция из катионита ионами водорода до полного изменения ионной формы ионита. [7]
Если скорость процесса ионного обмена лимитируется только химическим процессом, то концентрации обменивающихся ионов в любых точках объемов ионита и раствора независимы от координат, поскольку диффузия и конвекция идут значительно быстрее химической реакции. [8]
Процесс ионообменной адсорбции зависит от сил взаимодействия ионита с ионами, концентрации обменивающегося иона, размеров обменивающихся ионов, возможности проникновения ионов в зерна ионита, свойств растворителя. На процессы ионного обмена влияют радиусы ионов, их объем и гидратация. Например, при малых концентрациях ионов в растворе при обычной температуре полнота обмена ионов возрастает с. [9]
В дальнейшем с целью упрощения вопроса мы ограничимся рассмотрением случая, когда концентрация обменивающихся ионов весьма мала по сравнению с общей концентрацией электролита. [10]
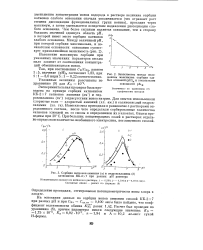 |
Зависимость между положением максимума сорбции слабых основаий ( рН м и показателем основности рКв.| Сорбция катионов аммония ( а и гидроксиламина ( б катионитом КБ-2Х7 при разных рН раствора. [11] |
Положение максимума сорбции при указанных значениях параметров весьма мало зависит от соотношения концентраций обменивающихся ионов. [12]
Следует подчеркнуть, что в логарифмических координатах можно представить не только область соизмеримых концентраций обменивающихся ионов, но и область малых концентраций одного из ионов как в твердой фазе, так и в растворе. При таком способе изображения результатов ионообменного равновесия возможно совместное рассмотрение результатов, изображаемых обычно отдельно в виде изотерм обмена и кривых титрования, и результатов исследования сорбции микрокомпонента на постоянном фоне макрокомпонента. [13]
Скорость установления равновесия зависит от гидродинамического режима жидкости ( скорости фильтрования), концентрации обменивающихся ионов, структуры зерен ионита, его проницаемости для ионов. Скорость ионного обмена определяется либо диффузией в пленке жидкости, либо диффузией в зерне ионита. Реакции обмена ионов протекают быстро, поэтому допустимы достаточно большие скорости фильтрования. [14]
ФА ФВ, N - Диффузионные потоки ионов; С, Съ - концентрации обменивающихся ионов, г-экв / л; CM - концентрация необменивающегося иона, е-экв / л; ф - потенциал; N - число Авогадро; Т - абсолютная температура; k - постоянная Больцмана; е - заряд электрона; е - диэлектрическая постоянная. [15]
Страницы: 1 2 3 4