Концентрация - органическая кислота
Cтраница 2
Интенсивное комплексование при этом идет преимущественно с двухвалентным железом и то только в начале процесса отмывки-пока величина рН, обычно повышающаяся в процессе отмывки, не достигнет неблагоприятных значений. С другой стороны, применение органической кислоты совместно с комплексоном позволяет ограничить концентрацию органической кислоты величиной, необходимой по условиям комплексования. [16]
Важной характеристикой промывочных растворов является способность связывать определенное количество железа - так называемая железоемкость растворов. Количество набираемого раствором железа зависит от ряда факторов: концентрации реагента, значения рН, температуры раствора, скорости его движения, формы нахождения оксидов железа в отложениях. Для определенного раствора большую роль играет тот или иной фактор, так, например, концентрация органических кислот предопределяет и скорость нарастания концентрации и максимальную концентрацию железа в растворе. [17]
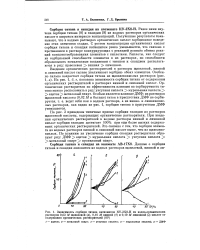 |
Зависимость сорбции титана катионитом КУ-2Х8-Н из водно-органических растворов 0 02 М щавелевой ( а, 0 10 М винной ( б и 0 10 М лимонной ( в кислот от содержания органических растворителей ( ОР. [18] |
Ранее нами изучена сорбция титана [8] и скандия [9] из водных растворов органических кислот в широком интервале концентраций. Полученные результаты показывают, что в водных растворах органических кислот сорбционное поведение этих элементов сходно. С ростом концентрации органических кислот сорбция титана и скандия катионитом резко уменьшается, что связано с протеканием в растворе конкурирующих с реакцией ионного обмена реакций комплексообразования элементов с кислотам: и. Кислоты, как следует из сорбционной способности элементов в их растворах, по способности образовывать комплексные соединения с титаном и скандием располагаются в ряд: щавелевая винная ] лимонная. [19]
Введенный в реакционную смесь готовый сульфат ртути каталитически не активен, что объясняется его практической не-растроримостью в винил ацетате. Ацетат ртути является менее активным катализатором реакции винилового обмена. Реакция винр-лового обмена принципиально отличается от реакции переэтери-фикации, в отличие от последней она не катализируется кислотами и основаниями. Скорость реакции винилового обмена пропорциональна концентрации органической кислоты и катализатора и не зависит от концентрации винилацетата. Во время реакции виниль-ная группа в в нилацетате не претерпевает никаких изменений и переносится к кислороду нуклеофильного реагента. Последний взаимодействует с органической кислотой с образованием циклического комплекса. [20]
Если полученный электролит имеет рН выше требуемого, то снижение кислотности производится добавкой органической кислоты. Эти электролиты работают с нерастворимыми анодами и поэтому концентрация золота падает; нормальная работа электролита возможна только до содержа-ния золота 1 0 - 1 5 г / л, после чего осадки становятся матовыми, после корректировки электролита и доведения концентрации золота до 2 5 - 3 5 г / л электролит начинает работать нормально. При высокой концентрации золота - в электролите ( выше 5 г / л) получаются напряженные растрескивающиеся осадки. Содержание присадок металлов меняется мало, концентрацию органической кислоты определяют измерением рН, при ее повышении добавляют органическую кислоту в виде концентрированного раствора. После корректировки ванны качество покрытия улучшается. [22]
Органические кислоты вызывают скорее равномерную, чем питтинговую коррозию, которая связана с действием углекислого газа. Скорость коррозии стали, вызываемой органическими кислотами, уменьшается со временем; реакция эта самоподавляющаяся. Кроме того, и, возможно, наиболее важным является то, что концентрация органических кислот весьма мала по сравнению с концентрацией углекислого газа. Шок и Сэдбери нашли также, что в присутствии кислот жирного ряда агрессивное действие углекислого газа проявляется при более низких концентрациях, чем в их отсутствие. [23]
Страницы: 1 2
