Концентрация - комплекс
Cтраница 1
Концентрация комплексов, следовательно, пропорциональна общей поверхности, которая может быть занята комплексами, концентрации алкилов в растворе и отношению суммы состояний свободного и связанного в комплексы металлалкила, которое может быть выражено в виде exp ( - - Dc / RT), где Dc - энергия диссоциации комплекса. Vc определяет скорость расходования мономера [ см. уравнение ( 11) ], следует ожидать, что в случае избытка MX скорость превращения будет пропорциональна концентрации алкила. И действительно, Гудман и Марк [161] нашли, что начальная скорость расхода этилена или пропилена пропорциональна концентрации триизобутилалюминия при условии, что большие количества TiCH3 связаны в комплекс с малым количеством алкила, добавляемого в виде разбавленного раствора в октане. Кроме того, оказалось, что по мере увеличения дисперсности галогенида металла и, следовательно, удельной поверхности TiCJ3, доступной для комплексо-образования, скорость расхода мономера возрастает. Наличие экспоненциальной зависимости характеризует влияние температуры на равновесие образования комплексов и показывает, что их концентрация будет, как правило, уменьшаться с увеличением температуры. [1]
Концентрация комплекса С0а - величина того же порядка, что и концентрация хлорофилла. Хлорофилл составляет 5 % от сухого веса Chlorella ( см. гл. Однако акцептор - не хлорофилл, так как водный клеточный экстракт, который содержит весь поглощенный в темноте радиоактивный углерод, бесцветен. Кроме того, клетки с различным содержанием хлорофилла не обнаруживают различий в абсорбирующей способности С 02 и этиолированные растения также способны поглощадь двуокись углерода. [2]
Концентрация комплекса в этих равновесиях ( вероятно, Fe2Cl6) должна быть чрезвычайно малой, чтобы можно было объяснить линейную зависимость, упомянутую выше. По аналогии с другими растворителями, описанными в этой работе, первое равновесие предпочтительно. [3]
Концентрация комплексов, вычисленная на основании уравнения ( 42), относится к комплексам, движущимся в обоих направлениях, и равна поэтому удвоенной концентрации комплексов, переходящих слева направо. [4]
Концентрация комплекса MeL / на поверхности электрода описывается зависимостью, сходной с уравнением ( 14 19); только у символов концентраций появляются нижние индексы О. Это не касается концентрации [ Ы, поскольку, как и раньше, мы полагаем, что она велика и остается постоянной независимо от места в исследуемой системе. Мы принимаем также, что коэффициенты активности у поверхности электрода такие же, как и в глубине раствора. [5]
Концентрация комплекса Zn ( Ox) всегда мала. [6]
Концентрация комплекса ск в объеме раствора электролита принимается равной нулю. [8]
Концентрацию комплекса [ Fe ПАН ] ХЛ находили из построенной отдельно зависимости окраски экстракта комплекса от концентрации железа. [9]
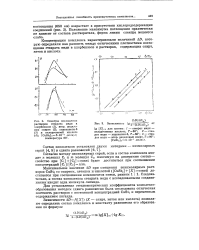 |
Спектры поглощения растворов стеарата меди в хлорбензоле ( 1, втор, децило-вом спирте ( 2, ундеканоне-6 ( 3 и иеларгоновой кислоте ( 4. [ CuSt2 ] o 5 - 10 - 3 молъ / л. температура 60. [10] |
Концентрацию комплекса характеризовали величиной AD, которую определяли как разность между оптическими плотностями поглощения стеарата меди в хлорбензоле и растворах, содержащих спирт, кетон. [11]
Концентрацию комплекса измеряли спектрофотометрически. [13]
Если концентрация комплексов или лигандов, которые участвуют в электродной реакции, изменяется со временем вследствие медленного протекания гомо - или гетерогенной химической реакций, то потенциал электрода зависит от времени, причем вид этой зависимости определяется кинетическими параметрами медленной реакции. Последние могут быть установлены из зависимости потенциала электрода от времени, если медленная реакция практически не нарушает равновесия стадии переноса электронов от реагирующих частиц к электроду и в противоположном направлении. Выражение для зависимости подобных квазиравновесных электродных потенциалов от времени можно получить, подставив в уравнение Нернста зависящие от времени концентрации частиц, которые выражены через кинетические параметры медленной химической реакции и время ее протекания. [14]
 |
Графическая проверка уравнения предельного катататиче-ского тока [ уравнения ( 166 - ( 170 ( а и ( 378 ( и 379 ( б ] восстановления Gam в присутствии SCN - ионов. [15] |
Страницы: 1 2 3 4