Концентрация - активный комплекс
Cтраница 1
Концентрация активных комплексов уменьшается. [1]
Поскольку концентрация активного комплекса составляет лишь малую долю от концентрации исходных веществ, даже ничтожное количество катализатора часто меняет кинетические свойства системы. Например, для заметного изменения скорости окисления сернистокислого натрия в водном растворе достаточно 10 - 13 г-экв катализатора ( сернокислой меди) на 1 л раствора. [2]
Поскольку концентрация активного комплекса составляет лишь малую долю от концентрации исходных веществ, даже ничтожное количество катализатора часто меняет кинетические свойства системы. Например, для заметного изменения скорости окисления сернистокислого натрия в водном растворе доста точно 10 - 13г - экв катализатора ( сернокислой меди) на 1 л раствора. [3]
Обозначим через сак концентрацию активных комплексов в интервале б на координате реакции. [4]
Общая скорость процесса пропорциональна концентрации активного комплекса. [5]
 |
Изменение энергии реакции. [6] |
Для вычисления константы скорости реакции, концентрация активного комплекса, находящегося в равновесии с реагирующими молекулами при их концентрации, равной единице, умножается на скорость, с которой активный комплекс пересекает барьер Б и падает в В. [7]
Из формулы ( 3) тем не менее видно, что концентрация активных комплексов зависит не столько от концентрации катализатора, сколько от его термодинамической активности и отношения коэффициентов активности мономера и комплекса. [8]
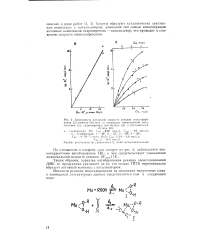 |
Зависимость начальной скорости реакции эпоксидирования 2 3-диметил - 2-бутсна от начальных концентраций катализатора ( а, гидроперекиси трст-бутила ( б и 2 3-диметил - 2. [9] |
Спирты образуют каталитически неактивные комплексы с катализатором, уменьшая тем самым концентрацию активных комплексов гидроперекись - - катализатор, что приводит к снижению скорости эпоксидирования. [10]
Очевидно, что скорость ферментативной реакции в присутствии ингибитора будет определяться концентрацией активного комплекса [ ES ], а она, в свою очередь - концентрацией ингибитора [ I ], константой ингибитора / Q и кинетическими константами самой ферментативной реакции. Количественная оценка действия ингибитора может быть дана путем расчета Kt по экспериментально определяемой скорости реакции в присутствии ингибитора при известных концентрациях реагирующих веществ. [11]
Из - формулы ( 3) тем не менее видно, что концентрация активных комплексов зависит не столько от концентрации катализатора, сколько от его термодинамической активности и отношения коэффициентов АКТИВНОСТИ мономера и комплекса. [12]
 |
Изменение потенциальной энергии системы при реакции типа AB D - - - - A BD. [13] |
Здесь речь идет, конечно, не о действительном равновесии, а о том, что концентрация активного комплекса считается такой же, какая была, бы при таком равновесии. [14]
Скэтчард [1] приходит к заключению, что не имеет значения, выражается ли скорость реакции через концентрацию активных комплексов или же рассчитывается через число соударений, при которых осуществляется требуемая ориентация и энергия столкновения достигает требуемой величины, после чего число соударений умножается на фактор, учитывающий длительность столкновения. Если молекулы получили требуемую энергию и в достаточной степени деформированы и правильно ориентированы еще до соударения, реакция будет происходить при каждом столкновении. Если же молекулы сталкиваются еще до того, как успела осуществиться одна из этих предварительных стадий, тогда будет справедлива модель предварительного образования комплекса. [15]
Страницы: 1 2