Концентрация - активный комплекс
Cтраница 2
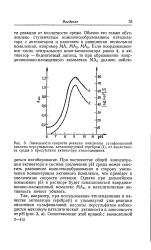 |
Зависимость скорости реакции окисления сульфаниловой кислоты персульфатом, катализируемой серебром ( I, от кислотности среды в присутствии активатора этилендиамина. [16] |
При постоянстве общей концентрации активатора в системе увеличение рН среды может сместить равновесие комплексообразования в сторону увеличения концентрации активного комплекса, что приведет к увеличению скорости реакции. [17]
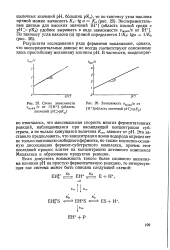 |
Схема зависимости.| Зависимость г макс / & от [ Н ] ( область значений. [18] |
Это заставило предположить, что концентрация ионов водорода определяет не только ионизацию свободного фермента, но также кислотно-основную диссоциацию фермент-субстратного комплекса, причем этот последний процесс влияет на концентрацию активного комплекса Михаэлиса и образование продуктов реакции. [19]
Скорость реакции пропорциональна концентрации активного комплекса са. [20]
Другим допущением теории является предположение о том, что активный комплекс можно считать находящимся в равновесии с исходными веществами. Здесь речь идет, конечно, не о действительном равновесии, а о том, что концентрация активного комплекса считается такой же, какая была бы при его равновесии с исходными веществами. Это предположение подтверждается совпадением рассчитанных с его помощью скоростей химических реакций с данными опыта и с результатами расчетов, не использующих предположение о равновесии. [21]
В теории абсолютных скоростей реакции ( TAG) понятия активного комплекса А и переходного состояния А совпадают. При выводе уравнения (V.174) в отличие от TAG и теории РРКМ предполагается, что переходное состояние А доступно экспериментальному исследованию, например, методами пикосекундной спектроскопии, если достаточно велика концентрация активных комплексов в растворе. [22]
Все реакции ( некаталитические и каталитические) протекают, как было показано ранее, через образование промежуточных комплексов или переходных состояний. В гомогенных некаталитических процессах промежуточный комплекс состоит из исходных молекул реагирующих веществ; в гомогенно-каталитических - из исходных молекул и атомно-молекулярных частиц катализатора; в гетерогенно-каталитических реакциях такой комплекс образуется на границе раздела фаз и представляет собой поверхностное химическое соединение. Концентрация активного комплекса в реакциях обычно чрезвычайно мала. [23]
Однако в действительности и то и другое основывается на одних и тех же принципах. Теория переходного состояния дает возможность понять эту точку зрения. Концентрация активных комплексов определяется равновесием с молекулами реагирующего вещества. [24]
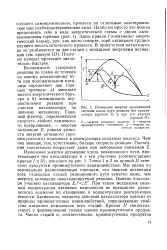 |
Изменение энергии реакционной системы вдоль пути реакции без катализатора ( кривая / и при его участии. [25] |
Точки / и 2 на кривой / / отвечают продуктам промежуточного взаимодействия. Мы видим по вертикально расположенным стрелкам, что энергия активации всех отдельных стадий реакционного пути заметно ниже, чем энергия активации некатализируемой реакции. При таком механизме реакции концентрация активных комплексов не превышает равновесного значения по отношению к концентрации реагирующих веществ. [26]
В основе ее лежит введенное Эйрингом понятие активного комплекса. По этому методу химическая реакция протекает через образование молекулами реагирующих веществ активного комплекса, находящегося в статистическом равновесии с ним. Основываясь на этом и сопоставляя различные возможные активные комплексы, можно выявить большую или меньшую их достижимость и определить в результате энергетически наиболее выгодный путь реакции. Легко видеть, что чем больше концентрация активного комплекса, тем больше и скорость образования продуктов реакции. Таким образом, скорость реакции определяется концентрацией этого комплекса Б рассматриваемый момент времени. [27]
За основу возьмем, что скорость реакции пропорциональна ( равна) скорости распада активного комплекса. Комплекс распадается по одной из связей, причем вероятность распада пропорциональна частоте колебаний по этой связи. Действительно, распад начинается в тот момент, когда колеблющиеся атомы находятся на максимальном расстоянии друг от друга. Кроме того, скорость реакции, очевидно, пропорциональна концентрации активного комплекса. [28]
Страницы: 1 2