Концентрация - комплексон
Cтраница 2
Приводятся методика микроэлектрофоретиче-ских измерений и результаты опытов влияния рН и концентрации комплексона III на электрофоретическую подвижность продуктов коррозии. [16]
На основании результатов проведенных экспериментов по изучению влияния рН среда, концентрации комплексона та железа, промотируь-щих добавок, температуры на поглотительную способность, селективность, стабильность и коррозионную активность разработан новый аффективный абсорбент для окисления сероводорода. Применяемый абсорбент отличается от аналогов высокой активностью, селективностью, низкой токсичностью и коррозионной агрессивностью по отношению к углеродистой стали. [17]
Прочность комплексов, образуемых с комплексонами, существенно выше, а поэтому концентрация комплексона не влияет на полноту реакции, комплексен в отмывочном растворе может быть израсходован полностью и концентрация его должна рассчитываться исходя только из стехиометрических соотношений. Совместное действие комплексона и органической кислоты позволяет снять упомянутое выше ограничение в отношении органической кислоты. [18]
III при определении кальция, мл; k - поправка для приведения концентрации комплексона к точно 0 05 М; l / i - объем пробы, взятой для определения жесткости, мл; V % - объем пробы, взятой для определения кальция, мл; 0 05 - молярность раствора комплексона III; 12 16 - эквивалент М § 2 -иона при ацидиметрическом титровании. [19]
При потенциале электрода 1 - 1 2 В достигается предельный ток, пропорциональный концентрации комплексона. [20]
 |
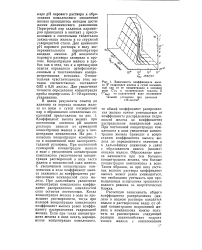
Зависимость средней электрофоре. [21] |
Результаты опыта представлены на рис. 3 в виде зависимости средней электрофоретичес-кой подвижности от концентрации комплексона. Как видно, с увеличением концентрации комплексона в питательной воде электрофоретичес-кая подвижность частиц продуктов коррозии возрастает. При этом знак заряда частиц продуктов коррозии остается отрицательным. [22]
При потенциале электрода 1 - 1 2 В достигается предельный ток, пропорциональный концентрации комплексона. [23]
Об этом свидетельствуют не только снижение концентраций тяжелых металлов в растворе, но и возрастание концентраций комплексона в нем. Этот же процесс ( операция в) для больших объемов требует 4 - 6 ч, а иногда и суток. [24]
Как следует из рис. 15 - 7, в данном случае для проведения отмывки на ходу концентрации комплексона в питательной воде должны быть не менее 1 мг / кг. [25]
Коэффициент выноса железа при постоянном значении рН водного раствора зависит от суммарной концентрации железа в воде и концентрации комплексона. На рис. 1 нанесена концентрация комплексона в подпиточной воде экспериментальной установки. При постоянной суммарной концентрации железа в воде с увеличением концентрации комплексона увеличивается концентрация растворенной в воде части железа и комплексной соли железа. С увеличением концентрации комплексона в воде коэффициент выноса снижается до коэффициента распределения комплексной соли железа. При дальнейшем увеличении концентрации комплексона коэффициент распределения комплексной соли остается постоянным. Когда концентрация железа в воде не превышает растворимости, тогда при нулевой концентрации комплексона коэффициент выноса равен коэффициенту распределения гидроокисей железа. [27]
 |
Растворимость ЭДТК итее натриевых солей в воде. [28] |
При исследовании в МЭИ термической стойкости трех растворов - Na2H2Y, Na4Y и Na4Y - с добавкой NaOH ( концентрация комплексона 300 мг / кг, температура 175 и 200 С) была установлена не только более высокая термическая стойкость Na4Y в сравнении со стойкостью NaoH Y, но, что примечательно, и еще большая устойчивость третьего раствора Na4Y - f - NaOH. [29]
Этилендиаминтетрауксусная кислота окисляется на вращающемся платиновом аноде в кислой и щелочной средах, образуя четкую волну, высота которой пропорциональна концентрации комплексона III и зависит от рН раствора. При рН 4 волна имеет горизонтальную площадку при 0 8 - 1 0 в, а в щелочной среде - при 0 45 - 0 65 в. Слабощелочной раствор соли кобальта титруют раствором комплексона III с платиновым вращающимся анодом при потенциале 0 55 - 0 60 в. Кривая титрования имеет V-образную форму. [30]
Страницы: 1 2 3 4